 元素周期律化学键1.docx
元素周期律化学键1.docx
- 文档编号:2562933
- 上传时间:2023-05-04
- 格式:DOCX
- 页数:14
- 大小:137.92KB
元素周期律化学键1.docx
《元素周期律化学键1.docx》由会员分享,可在线阅读,更多相关《元素周期律化学键1.docx(14页珍藏版)》请在冰点文库上搜索。
元素周期律化学键1
【基础知识】
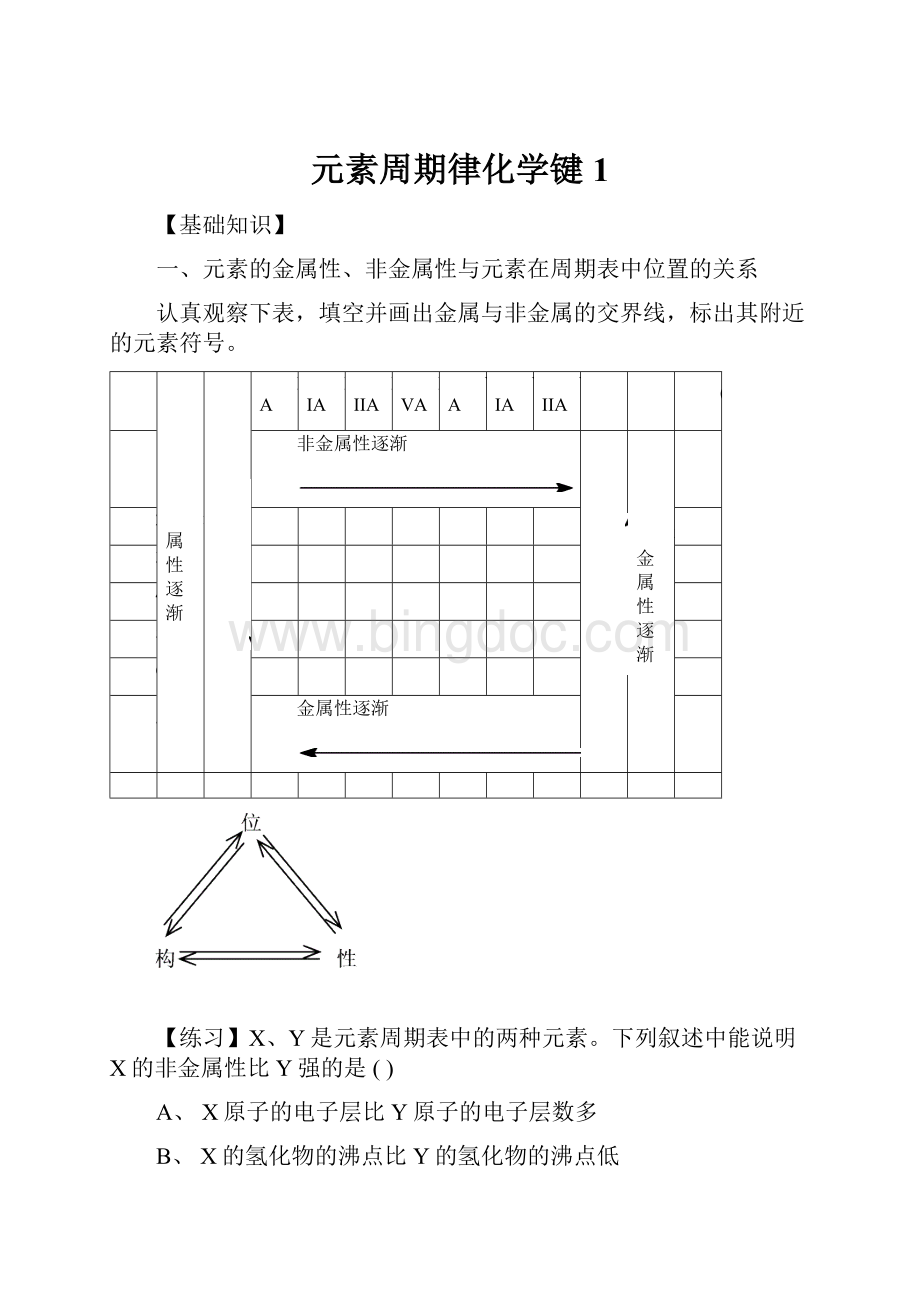
一、元素的金属性、非金属性与元素在周期表中位置的关系
认真观察下表,填空并画出金属与非金属的交界线,标出其附近的元素符号。
金属性逐渐
IA
IIA
IIIA
IVA
VA
VIA
VIIA
0
1
非金属性逐渐
非金属性逐渐
2
3
4
5
6
7
金属性逐渐
【练习】X、Y是元素周期表中的两种元素。
下列叙述中能说明X的非金属性比Y强的是()
A、X原子的电子层比Y原子的电子层数多
B、X的氢化物的沸点比Y的氢化物的沸点低
C、X的气态氢化物比Y的气态氢化物稳定
D、Y的单质能将X从NaX的溶液中置换出来
二、元素的化合价与元素在周期表中位置的关系
思考:
1、标出下列有下划线元素的化合价:
NaClMgCl2AlCl3H2SiO3H3PO4H2SO4HClO4
2、总结最高正化合价与什么有直接关系?
___________________________________________________________________
得出结论:
主族元素最高正化合价===
思考:
写出下列化合物中有下划线元素的化合价:
Na2CO3与CH4H2SO4与H2SHCl与HClO4分析最高正化合价与最低负化合价之间的关系,并解释其原因。
得出结论:
【练习】某元素X的最高价氧化物对应水化物的化学式为HXO4,则其气态氢化物的化学式为:
;
若其水溶液呈现酸性,且能与AgNO3溶液反应生成白色沉淀,则它在元素周期表中的位置是:
。
三、元素周期律、元素周期表的应用
1、预测未知物的位置与性质
【练习】Ra(镭)是原子序数最大的第ⅡA族元素,下列说法不正确的是()
A、原子半径是第ⅡA族中最大的
B、遇冷水能剧烈反应
C、位于第七周期
D、Ra(OH)2是两性氢氧化物
2、寻找所需物质
在能找到制造半导体材料,如;
在能找到制造农药的材料,如;
在能找到作催化剂,耐高温,耐腐蚀的合金材料。
【自主探究】
(08年海南高考卷)根据元素周期表1—20号元素的性质和递变规律,回答下列问题。
(1)、属于金属元素的有________种,金属性最强的元素与氧反应生成的化合物有___________(填两种化合物的化学式);
(2)、属于稀有气体的是___________(填元素符号,下同);
(3)、形成化合物种类最多的两种元素是__________________;
(4)、第三周期中,原子半径最大的是(稀有气体除外)___________;
(5)、推测Si、N最简单氢化物的稳定性_____大于_____(填化学式)。
例1.下列说法中正确的是()
A.非金属元素呈现的最高化合价不超过该元素原子的最外层电子数
B.非金属元素呈现的最低化合价,其绝对值等于该元素原子的最外层电子数
C.最外层有2个电子的原子都是金属原子
D.最外层有5个电子的原子都是非金属原子
1.某元素x的最高价含氧酸的化学式为HnXO2n-2:
,则在某气态氢化物中,x元素的化合价为()
A.一(12—5n)B.一(12—3n)
C.一(6—3n)D.一(10一n)
2.X、Y、Z三种元素原子具有相同的电子层数,x的最高价氧化物对应水化物呈碱性,Y的最高价氧化物对应水化物呈酸性,而z的最高价氧化物对应水化物呈两性,则它们的原子序数逐渐增加的顺序是()
A.X、Y、ZB.X、Z、Y
C.Z、Y、XD.Y、Z、X
3.下列叙述能说明金属A比金属B更活泼的是()
A.A原子的最外层电子数比B原子的最外层电子数少
B.A原子的电子层数比B原子多
C.1molA从酸中置换出的H:
比lmolB多
D.常温下,A能从水中置换出氢气,而B不能
例2.元素A、B的原子序数都小于18,已知A元素原子的最外层电子数为a,次外层电子数为b;B元素原子的M层电子数为(a一b),L层电子数为(a+b),则A、B两元素所形成的化合物的性质可能有()
A.能与水反应B.能与硫酸反应
C.能与NaOH反应D.能与碳酸钠反应
1、短周期元素E的氯化物ECln的熔点为-78℃,沸点为59℃;若0.2molECln与足量的AgNO3溶液完全反应后可以得到57.4g的AgCl沉淀。
下列判断错误的是()
A.E是一种非金属元素B.在ECln中E与Cl之间形成共价键
C.E的一种氧化物为EO2D.E位于元素周期表的IVA族
2、下列说法正确的是()
A.SiH4比CH4稳定B.O2―半径比F―的小
C.Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强
D.P和As属于第ⅤA族元素,H3PO4酸性比H3AsO4的弱
3、下列叙述中正确的是()
A.除零族元素,短周期元素的最高化合价在数值上都等于该元素所属的族序数
B.除短周期外,其他周期均有18个元素
C.副族元素中没有非金属元素
D.碱金属元素是指ⅠA族的所有元素
化学键
一.离子键
情景:
NaCl的形成:
写出Na原子、Cl原子的结构示意图:
、;
Na、Cl原子要达到8电子稳定结构,Na原子需要,而Cl原子则要电子。
用图示表示如右:
1.离子键:
概念:
之间的叫做离子键。
(1)成键微粒:
和。
(2)成键实质:
相互作用(包含吸引和排斥):
接近到某一定距离时,和作用达到平衡就形成了离子键。
(3)成键条件:
通常是活泼金属元素(ⅠA、ⅡA)与活泼非金属元素(ⅥA、ⅦA)间。
2.离子化合物:
概念:
像NaCl这种只要含离子键的化合物叫做离子化合物。
(1)常见的离子化合物:
①活泼金属氧化物:
如CaO、Na2O、Na2O2、K2O等;
②强碱:
如NaOH、KOH、Ba(OH)2、Ca(OH)2等;
③绝大多数盐:
如Na2CO3、BaSO4、NH4Cl等。
(2)物理性质主要特点:
通常有熔、沸点,硬度,熔化后导电。
(3)规律:
离子键只存在离子化合物中,离子化合物中一定含有离子键
【练习】:
1.下列原子序数所对应的元素组中,两者能以离子键结合成稳定化合物的是()
A.1和17B.12和9C.14和6D.15和8
2.下列物质由离子构成的是()
A.Cl2B.CO2C.HClD.MgCl2
3.电子式
电子式:
在元素符号周围用“·”或“×”来表示原子的最外层电子(价电子)的式子叫电子式。
(1)原子的电子式:
NaMgAlSiPSClAr
(2)离子的电子式:
①阳离子:
单核金属阳离子的电子式:
一般直接用表示,如:
等。
常见复杂阳离子的电子式:
如:
NH
:
H3O+:
②阴离子:
单核非金属阴离子的电子式:
如:
Cl-:
S2-:
H-:
O2-:
常见复杂阴离子的电子式:
如:
OH-:
O
:
C
:
规律总结:
单核金属阳离子的电子式就是其
复杂阳离子及阴离子的电子式均要做到“二标”:
即标“”和“”
(3)离子化合物的电子式(即阴、阳离子的电子式的结合式):
AB型:
如NaCl__________________MgO______________NH4Cl
A2B型:
如Na2O_________________K2S
AB2型:
如MgCl2_______________CaH2
其他型:
如KOHBa(OH)2Na2O2
(4)用电子式表示离子化合物形成过程:
+ ×Mg× +
—→[
]- Mg2+[
]-
规律总结:
用箭头标明电子转移方向;相同的离子单个写;连接用“→”不用“=”。
(1)什么是离子键?
哪些元素化合时可形成离子键?
(2)用电子式表示形成过程:
NaCl:
CaF2:
(3)以氢分子、氯化氢分子为例,分析非金属元素之间的化学键的形成过程:
H2:
HCl:
2、共价键:
1、概念:
叫做共价键。
(1)成键微粒:
(2)成键实质:
非金属元素的原子易得电子,故非金属元素的原子间形成化学键时一般不发生电子的,通常通过形成化学键。
(3)共价键的分类:
按共用电子对是否偏移分:
①非极性共价键:
②极性共价键:
按共用电子对情况分:
单键、双键、叁键
(4)共价键的表示法:
电子式:
物质的电子式,如HCl:
物质形成过程的电子式,如H2O:
结构式:
在化学上,用表示的图式叫做结构式。
如:
H2:
H-H
练习:
表示Cl2、H2O、NH3、H2S、CO2、HClO分子的形成过程:
Cl2O2N2
NH3CO2HClO
2、共价化合物
(1)概念:
只含有共价键的化合物叫共价化合物。
如H2O、CO2、SiO2、CH3CH2OH、HCl等。
(2)物理性质主要特点:
通常有熔、沸点,硬度,熔化后导电。
三、化学键
(1)定义:
使相结合或相结合的通称为化学键。
(3)化学反应的实质:
物质发生化学变化的过程就是旧化学键与新化学键的过程。
四、《科学视野》分子间作用力与氢键
(1)分子间作用力
①概念:
分子之间存在着一种把分子叫做分子间作用力,又称
②强弱:
分子间作用力比化学键,它主要影响物质的、等物理性质,而化学键属分子内作用力,主要影响物质的
③存在:
分子间作用力只存在于由分子组成的共价化合物、共价单质和稀有气体的分子之间。
(注:
稀有气体由单原子分子构成,其分子内不存在化学键,只存在分子间作用力)
④规律:
一般来说,对于组成和结构相似的物质,越大,分子间作用力,物质的熔点、沸点也越。
如:
HCl〈HBr
(2)氢键①概念:
像、、等这些分子之间还存在着一种比的相互作用,这种相互作用叫做氢键
②对物质性质的影响:
分子间形成的氢键会使物质的熔点和沸点,这是因为固体熔化或液体汽化时必须破坏分子更强间的氢键,从而消耗更多的能量。
例1.下列物质中属于离子化合物的是()
A.苛性钠B.碘化氢C.硫酸D.醋酸
1.下列表示电子式的形成过程正确的是()
2.下列说法正确的是()
A.离子键就是使阴、阳离子结合成化合物的静电引力
B.所有金属与所有非金属原子之间都能形成离子键
C.在化合物CaCl2中,两个氯离子之间也存在离子键
D.含有离子键的化合物一定是离子化合物
3.下列指定微粒的个数比为2:
1的是()
A.Be2+中的质子和电子
B.
原子中的中子和质子
C.NaHC03中的阳离子和阴离子
D.BaO2(过氧化钡)固体中的阴离子和阳离子
例2.下列叙述中正确的是()
A.阳离子一定是金属离子,阴离子一定只含有非金属元素
B.某金属元素的阳离子和某非金属元素的阴离子组成的物质一定是纯净物
C.阴、阳离子相互作用后一定形成离子化合物
D.金属K不能从盐的水溶液中置换出金属单质
1下列关于离子键的说法中正确的是()
A.离子键是由阴、阳离子通过静电作用达到平衡时形成的
B.只有金属和非金属化合时才能形成离子键
C.凡是含有离子键的化合物一定含有金属元素
D.含有离子键的化合物一定是离子化合物
2.下列化合物的电子式书写正确的是()
3、.下列关于离子化合物的叙述正确的是()
A.离子化合物中都含有离子键
B.离子化合物中的阳离子只能是金属离子
C.离子化合物如能溶于水,其水溶液一定可以导电
D.溶于水可以导电的化合物一定是离子化合物
4、下列性质中,可以证明某化合物内一定存在离子键的是()
A.可溶于水B.具有较高的熔点
C.水溶液能导电D.熔融状态能导电
5、下列关于电子式的说法不正确的是()
A.每种元素的原子都可以写出电子式
B.简单阳离子的电子式与它的离子符号相同
C.阴离子的电子式要加方括号表示
D.电子式就是核外电子排布的式子
例3、用电子式表示。
①铝原子_________________②硫离子_________________
③硫化钾的形成过程
1、某化合物XY2中,各离子的电子层结构相同,且电子总数为54,则XY2的化学式为________________,电子式为________________。
2、X元素位于ⅡA族,原子核内有12个中子,它在最高价氧化物中的质量分数是60%,Y元素原子的原子核外有9个电子,X与Y能形成稳定化合物,该化合物的化学式是________,它是通过________键结合的,它形成过程的电子式为____________。
例4.HBr分子的电子式为()
A.H
B.H+ Br-C.H+ [
]-D.H—Br
1.下列化合物的电子式书写正确的是()
A.K
B.H∶
C.Na+ [
]2- Na+D.H+ [
]-
2.关于化学键的下列叙述中,不正确的是()
A.离子化合物可能含共价键
B.共价化合物可能含离子键
C.离子化合物中一定含离子键
D.共价化合物中一定不含离子键
3.某元素的原子最外层只有1个电子,它跟卤素结合时,所形成的化学键()
A.一定是离子键B.一定是共价键
C.可能是离子键,也可能是共价键D.以上说法都不正确
例5.已知乙醇分子内含有C—C键,则固体乙醇分子中不存在的作用力是()
A.离子键B.极性键C.非极性键D.范德华力
1.下列分子结构中,原子的最外层电子不能满足8电子稳定结构的是()
A.CO2B.PCl3C.SiF4D.NO2
2下列过程中,共价键被破坏的是()
A.碘升华B.溴蒸气被木炭吸附
C.酒精溶于水D.HCl气体溶于水
例6.短周期元素E的氯化物ECln的熔点为-78℃,沸点为59℃;若0.2 molECln与足量的AgNO3溶液完全反应后可以得到57.4 g的AgCl沉淀,下列判断错误的是()
A.E是一种非金属元素
B.在ECln中E与Cl之间形成共价键
C.E的一种氧化物为EO
D.E位于元素周期表的ⅡA族
1.下列物质中:
①CS2②Ar③CaH2④N2⑤NH4Cl⑥Mg(OH)2⑦F2⑧HF⑨H2SO4⑩Na2O2则:
⑴只有非极性键的是;⑵只有极性键的是;⑶只有离子键的是;
⑷既有离子键,又有非极性键的是;⑸既有离子键,又有极性键的是;
⑹不含化学键的是;⑺属于共价化合物的;⑻属于离子化合物的是。
课下作业
在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol XY2含有54 mol电子。
该融雪剂的化学式是_____;X与氢元素形成化合物的电子式是,其与水反应产生氢气的方程式是
元素D、E原子的最外层电子数是其电子层数的2倍,且D与Y相邻,则D的离子符号为_______;D所在族元素的氢化物中,沸点最低的是(填化学式);D、E元素形成稳定化合物的结构式是。
元素W与Y同周期,与E同族;元素Z的单质分子Z2中存在共价叁键;W与Z能形成一种耐高温的新型无机非金属材料,该材料的化学式是___________;Z原子与氢原子以1∶5形成的化合物中的含有化学键类型是。
元素R与Y同族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2,该反应的离子方程式为____________
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 元素周期律 化学键
 冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 建筑工程编制依据及概况.docx
建筑工程编制依据及概况.docx
