 蛋白质工程.docx
蛋白质工程.docx
- 文档编号:9187280
- 上传时间:2023-05-17
- 格式:DOCX
- 页数:37
- 大小:404.89KB
蛋白质工程.docx
《蛋白质工程.docx》由会员分享,可在线阅读,更多相关《蛋白质工程.docx(37页珍藏版)》请在冰点文库上搜索。
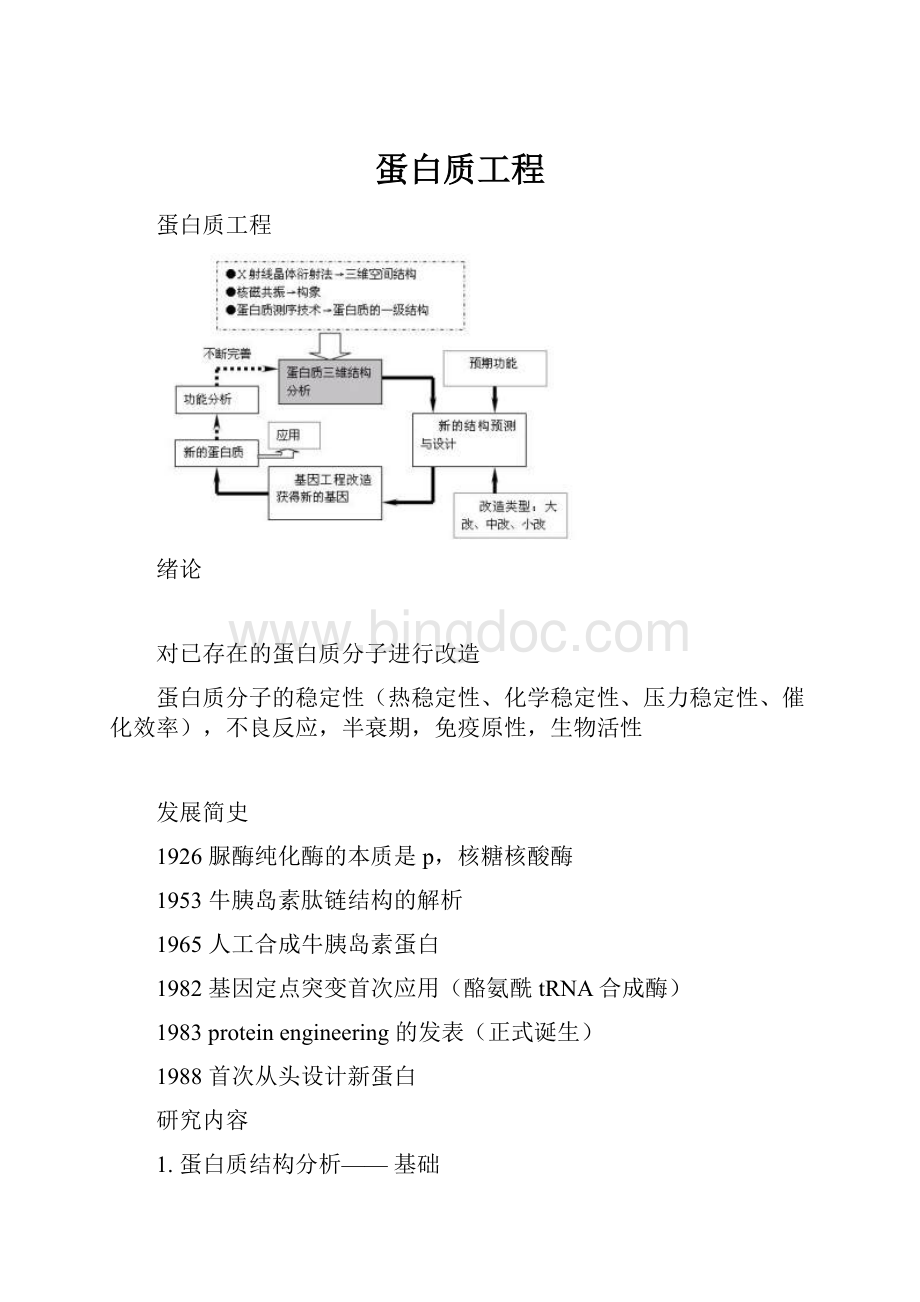
蛋白质工程
蛋白质工程
绪论
对已存在的蛋白质分子进行改造
蛋白质分子的稳定性(热稳定性、化学稳定性、压力稳定性、催化效率),不良反应,半衰期,免疫原性,生物活性
发展简史
1926脲酶纯化酶的本质是p,核糖核酸酶
1953牛胰岛素肽链结构的解析
1965人工合成牛胰岛素蛋白
1982基因定点突变首次应用(酪氨酰tRNA合成酶)
1983proteinengineering的发表(正式诞生)
1988首次从头设计新蛋白
研究内容
1.蛋白质结构分析——基础
2.结构、功能的设计和预测——基础的应用与验证
3.创造/改造蛋白质——新蛋白——终目标
应用:
抗病毒药β-干扰素稳定性的改进。
酪氨酰tRNA合成酶
改变酶的专一性
蛋白质的理化性质
一、热力学函数
内能:
组成物体的所有分子的无规则运动的动能与分子间相互作用的势能之和。
·焓:
是一个系统的热力学参数。
它描述的是体系的一个状态性质,它的改变量仅仅取决于系统的始态和终态,用符号H表示,即:
H=E+pV其中,E为系统内能,p为其压强,V则为体积。
·熵(S):
是度量体系混乱度的热力学函数。
从微观的角度来看,熵具有统计意义,它是体系微观状态数(或无序程度)的一种量度。
熵值小的状态,对应于比较有秩序的状态,熵值大的状态,对应于比较无秩序的状态。
·热力学第一定律:
能量既不能创生也不能消灭。
用数学方式表达为:
ΔU=0,其含义是,在任何隔离系统中系统储藏的能量不变。
能量守恒
·热力学第二定律:
自发过程向熵值(宇宙的总的混乱程度)增加的方向进行。
用数学方式表达为:
ΔS>0,其含义是,在任何隔离系统中,不违背第一定律的过程得以进行的最起码的条件是该系统的熵值增加。
吉布斯自由能(G):
亦称吉布斯函数,它是定温定压下系统的状态函数。
可以用公式表示为:
G=H-TS
其中,T为绝对温度;S为体系的熵。
当ΔG<0时,自发过程,被称为是放能的过程,它们可以用来做功;
当ΔG=0时,反应已达到平衡,即其正向过程和逆向过程正好处于平衡;
当ΔG>0时,非自发过程,被称为吸能的过程,必须注入自由能才能驱动此类过程。
稳定蛋白质三维结构的作用力:
氢键、范德华力、疏水作用力和盐键(离子键)及共价二硫键。
盐桥或离子键又称盐键,它是正电荷与负电荷之间的一种静电相互作用。
盐键的形成既是静电相互作用的过程也是熵增的结果。
·范德华力有三种来源:
取向力:
取向力是极性分子间的固有偶极同极相互排斥异极相互吸引,定向排列,产生分子间作用力。
诱导力:
诱导力是极性分子与非极性分子的固有偶极与诱导偶极间的作用力,它的大小与分子的极性和变形性等有关。
色散力:
色散力是非极性分子间瞬时偶极距的相互作用力。
范德华力包括吸引力和斥力。
相对作用力较弱的氢键在使线形蛋白折叠成能发挥生物活性的最稳定结构中有重要作用
疏水效应:
水介质中球状蛋白质的折叠总是倾向于把疏水残基埋藏在分子的内部。
这一现象被称为疏水作用或疏水效应.蛋白质溶液系统的熵增加(熵变化∆S为正值)是疏水作用的主要动力。
二硫键
又称S-S键是共价键。
是2个SH基被氧化而形成的-S-S-形式的硫原子间的键。
在生物化学的领域中,通常系指在肽和蛋白质分子中的半胱氨酸残基中的键。
为了确定蛋白质的一级结构,须在2-巯-乙醇、二硫苏糖类、巯基乙酸等的硫化合物与尿素等变性剂同时存在下将二硫键打开.
二硫键对肽链的正确折叠不是必要的,但它对稳定折叠态结构作出贡献。
RNA酶复性实验。
二、蛋白质折叠
(一)历程
二级结构的形成,稳定,多途径折叠,天然态的形成
(二)蛋白质折叠的速度机制
假定每个氨基酸残基可能的构象状态数为j,一个有N+1个氨基酸残基,N个肽单位的完全去折叠蛋白质,其肽链可能获得的构象状态数为jN。
例如j=8,一个有101个氨基酸残基的较小的蛋白质,其肽链的可能构象状态为8100(1089)。
如果构象之间的转换速率为k,蛋白分子经历全部构象的平均时间为:
τ=(Nk)-1jN
蛋白质的折叠不是一个随机过程,是通过特定的动力学途径达到天然构象,即动力学上最容易达到的构象
(三)蛋白质折叠热力学
蛋白质的折叠结构在一定条件下是热力学最稳定的,即通常的自由能极小的状态。
由熵函数和吉布斯自由能,简要分析蛋白质折叠结构原理。
(4)其它常见的折叠病
折叠病:
蛋白质分子的氨基酸序列没有改变,只是其结构或构象有所改变也能引起疾病。
老年性痴呆症、囊性纤维病变、家族性高胆固醇症、家族性淀粉样蛋白症、某些肿瘤、白内障等。
疯牛病-朊病毒:
致病蛋白-朊病毒蛋白(PrP)在脑组织中累积而引起的
(1)由一种称Prion的蛋白质的感染引起的
(2)致病Prion与正常Prion的一级结构完全相同,只是空间结构不同
(3)致病蛋白Prion通过蛋白分子间的作用,感染正常蛋白Prion转变为致病的折叠状态
(五)测定蛋白质构象的各种方法
方 法
提供的结构信息
主要指标
主要设备
应 用
核磁共振
溶液中蛋白质分子构象;构象动力学
化学位移,谱线强度,自旋偶合常数
脉冲傅里叶NMR波谱仪
越来越多
圆二色性光谱法
二级结构及其变化
椭圆度
圆二色性光谱仪
很多
荧光光谱
Tyr或Tyr微区;构象变化
发射光谱,量子产率
自动扫描荧光分光光度计
很多
紫外差示光谱法
Tyr或Tyr微区;构象变化
不同波长∆OD
双光路紫外分光光度计
很多
激光拉曼光谱法
二级结构
拉曼光谱峰
激光拉曼光谱仪
不成熟难应用
氢同位素交换
氢键数目,规则二级结构含量
与环境水不可交换的肽键氢的个数
红外分光光度计分子筛+氚测定
较少
X射线衍射结构分析
多肽链上所有原子的空间排布,但氢原子除外
衍射点的强度和位置
高分辨率X射线衍射仪
很多
小角中子衍射
多肽链上所有原子的空间排布
散射强度的分布
中子源;小角相机
刚起步
蛋白质的分子生物学改造:
——理性设计&非理性设计
一、蛋白质的化学修饰(理性设计)
(一)侧链基团修饰
1、氨基——赖氨酸的Σ氨基
1 氨基修饰剂:
三硝基苯磺酸(TNBS):
生成三硝基苯基化的氨基磺酸复合物,在420nm处能产生特定光吸收
2 氨基烷基化试剂:
卤代乙酸、芳香卤和芳香族磺酸
3 氨基甲氨酰化:
氰酸盐
4 赖氨酸氨基在中性pH下与磷酸吡哆醛(PLP)反应形成席夫碱后再用硼氢化钠还原,生成PLP衍生物。
在325nm处有最大吸收峰,可用于定量检测
2、羧基——谷氨酸和天冬氨酸残基,产物一般为脂类或酰胺类,水溶性的碳二亚胺
3、巯基
巯基有很强的亲核性,容易发生反应
烷基化试剂:
碘乙酸和碘乙酰胺
N-乙基马来酰胺:
产物在300nm处有最大吸收
5,5-二硫-2-硝基苯甲酸(DTNB)与巯基反应生成二硫键,释放1个2-硝基-5-硫苯甲酸阴离子,在412nm处有很强吸收峰
氧化:
过氧化氢与巯基形成二硫键,大量时形成磺酸,也可以生成次磺酸
4、二硫键的化学修饰
用过量的巯基乙醇将二硫键还原为游离巯基
鉴定有无及位置:
非还原、还原双向SDS电泳
5、其他
精氨酸的胍基-丁二酮
组氨酸的咪唑基-氮原子的烷基化或碳原子的亲核取代,焦炭酸二乙酯(DPC)-产物在240nm有吸收和碘代乙酸
色氨酸的吲哚基-N-溴代琥珀酰亚胺(NBS),280nm处光吸收减少
酪氨酸-四硝基甲烷(TNM)生成发色基团3-硝基酪氨酸衍生物
(二)蛋白质位点专一性修饰
1、亲和标记:
(不可逆抑制作用)酶活性部位
2、光亲和标记
(三)PEG修饰
蛋白质和PEG偶联的部位有:
氨基、羧基和巯基
功能
1掩盖蛋白质表面抗原决定簇→不与受体结合,不被机体免疫系统识别,避免相应抗原的产生,降低蛋白质的免疫原性
2大分子的屏障效应阻碍蛋白酶的降解
3减少肾小球的排出,
4半衰期延长
5改善蛋白质生物分布及溶解性能
(4)化学交联和化学偶联
交联:
分子亚基内部,多个蛋白质分子间形成网状交联,
偶联:
将一个蛋白质分子偶联到一个化学惰性水不溶性的生物大分子上,形成固定化蛋白质
--------------------------------------------------------------------------------------
获取目的基因片段的方法:
化学合成法
PCR法
基因文库法
cDNA文库法
目的基因转入宿主细胞
转化
转染
显微注射
电穿孔
重组子的筛选
抗生素抗性筛选法:
含拮抗抗生素表型的重组子可在含抗
生素环境生长
互补筛选法:
载体的表达产物与宿主细胞中营养缺陷型突
变发生互补作用
营养缺陷型筛选法:
载体携带某些营养成分的编码基因,只有含转化子的菌落才能够在缺少该营养物质的培养板上生长从而实现筛选
噬菌斑筛选法:
经噬菌体载体包装的外源重组DNA转染宿主细胞,转化子在固体培养板上出现清晰的噬菌斑
宿主细胞表达系统
原核:
大肠杆菌
真核:
酵母昆虫细胞、哺乳动物细胞
二、定点突变
(一)寡核苷酸引物突变
通过聚合酶的作用启动DNA分子进行复制,用含有突变碱基的寡核苷酸片段作引物合成DNA子链的一部分。
引物中除了所需的突变碱基之外,其余部分则应与目的基因编码链的特定区段完全互补.
①将待突变基因克隆到突变载体上;
②制备含待突变基因的单链模板;
③引物与模板退火5’端磷酸化的突变寡核苷酸引物,与待突变的核苷酸形成一小段碱基错配的异源双链的DNA
④合成突变链:
在DNA聚合酶的催化下,引物以单链DNA为模板合成全长的互补链,而后由连接酶封闭缺口,产生闭环的异源双链的DNA分子;
⑤转化和初步筛选异源双链DNA分子,转化大肠杆菌后,产生野生型、突变型的同源双链DNA分子。
可以用限制性酶切法、斑点杂交法和生物学法来初步筛选突变的基因;
⑥对突变体基因进行序列分析。
(二)PCR突变
1、重叠延伸PCR
四种扩增引物、三轮PCR反应
应用两个互补的并在相同部位具有相同碱基突变的内侧引物,扩增形成两条有一端可彼此重叠的双链DNA片段,两者在其重叠区段具有同样的突变。
两条双链DNA片段经变性和退火处理,形成两种不同形式的异源双链分子。
然后选用两个外侧寡核甘酸引物进行第三轮PCR扩增,可得到一种含有突变位点的突变体DNA。
2、大引物突变法:
三种扩增引物、两轮PCR反应
将第一轮PCR扩增产物作为第二轮PCR扩增引物
优缺点:
突变率高、需先连接载体、需测序确定突变
3、扩增环状质粒全长
用两个突变引物同时对质粒DNA扩增,扩增产物依次通过KpnI限制性内切酶酶切,PfuDNA聚合酶补平,T4DNA连接酶连接,转化大肠杆菌,筛选阳性克隆
(三)盒式突变
利用一段人工合成的含基因突变序列的寡核苷酸片段,取代野生型基因中的相应序列。
特点:
简单易行,突变率高,可以在一对限制酶切位点内进行一次突变而获得多个位点
缺点:
需存在酶切位点
非理性设计:
一、定向进化
不用事先了解酶的结构、活性位点、催化机制等各种因素,只需人为地控制进化条件,以希望模拟天然进化机制来达到体外对酶基因进行改造,产生基因多样性,并通过定向筛选或选择技术获取定向选择的具有特定性质的突变酶的目的。
基本原则:
获取你所筛选的突变体
定向进化=随机突变+定向选择
(一)易错PCR(error-pronePCR)
特点:
快速简便
能控制突变频率
使用低保真度的TaqDNA聚合酶或改变PCR常规的反应条件,引起碱基以某一频率进行随机错配而引入多点突变,构建突变库,选择或筛选出所需的突变体。
理论上每个靶基因导入的取代残基在1.5~5个之间
连续易错PCR
(二)DNA改组
原理:
用DNaseI或者超生波进行切割产生随机大小片段,再从正突变基因库中分离出来所需的DNA片段,得到的随机片段在不加引物的多次PCR循环中,彼此之间互为模板和引物进行扩增,直到连接成为接近目的基因长度的DNA分子,然后再利用基因两端序列为引物扩增获得全长基因。
特点:
能在较短时间内获得性能明显改善的酶蛋白
(三)随机引物体外重组法
以单链DNA为模板,配合一套随机序列引物,产生大量和模板不同位点互补的短片段,再进行PCR时,它们之间可以相互同源引导和重组进行合成。
特点:
突变率和重组频率可通过改变随机引物的长度、浓度、时间、温度及其它反应条件来控制。
(四)交错延伸法(StEP)
它是在PCR反应中,将含有不同点突变的模板混合,随之进行多轮变性、短暂的复性/延伸,反复重复直到形成全长基因片段。
特点:
1.缩短反应时间
2.新生DNA分子含有大量的突变组合
3.可通过控制反应条件和时间来进行调节
三、融合酶
主要是指将两个或多个酶分子组合在一起所形成的融合蛋白.
杂合酶,把不同酶中的部件有机的组合在一起从而在分子水平上出现了杂种优势
非理性设计法:
通过构建库,再从中筛选出所需要的融合体
理性设计法:
要求对操作对象的结构和功能有一个全面的了解,才能实现几个蛋白质的交换融合.
构建策略
注意:
蛋白质的融合通常在同系之间进行,因为同源蛋白质序列的相似性越低,融合后导致酶活性丧失的可能性越大,并且其动力学参数、底物专一性、热稳定性、最适pH等基本特性越易改变。
二级结构融合:
在融合酶中具有特定功能的二级结构的互换可以实现酶的某些性质的改变.例如:
谷胱甘肽还原酶和硫辛酰胺脱氢酶的辅助因子结合结构互换,实现了NADH和NADPH辅因子的互换.
功能域融合:
如果酶的活性部位位于不同的结构域上,可以通过功能域的程序化组合来生产新的融合酶。
整个酶蛋白的融合:
两个或多个酶蛋白融合在一起就可以产生具有多个功能的融合酶。
应用
理论研究方面
1.确定蛋白质结构与功能的关系
2.确定蛋白质之间的相互作用
实际应用方面
1.非催化特性的优化
2.创造新催化活性酶
3.研究酶及其它蛋白质的定位及移动
4.在酶内部创建别构作用
5.构建具有双催化活性的功能酶
蛋白质纯化
蛋白质纯化的一般程序
预处理将蛋白质从目的材料释放,天然状态影响蛋白至提取率和纯度
一、细胞破碎:
1、机械法
方法
适用范围
组织捣碎法
材料+液体捣碎
机械切力大,对大分子(核酸)提取有影响
匀浆法
组织-剪碎-置于管中--研棒来回研磨
适合少量组织和动物脏器组织。
丝状真菌,较小的阳性细菌等不合适
高压匀浆法
可产生高压的正向排代泵+排出阀
排出阀有狭窄的小孔,其大小可以调节。
细胞浆液进入泵体内,高压下在排出阀的小孔中高速冲出,射向撞击环上,由于突然减压和高速冲击,使细胞受到高的液相剪切力而破碎。
常用于酵母、细菌的破碎团状或丝状真菌,较小的革兰氏阳性,也不适合用该法处理
研磨法
加入石英沙、玻璃粉或其他研磨剂,进行研磨。
工业:
珠磨机。
罐体内装一定数量的钢球或瓷球玻璃珠随搅拌桨转动,使珠子与细胞之间产生了撞击和剪切效应,细胞破碎,释放出内含物。
在细胞匀浆液出口处设置了珠液分离器滞留珠子,使珠液分离破碎能够连续进行。
珠磨机破碎率较高的细胞,常用于生物药物的生产中。
振荡珠击破碎法
将等体积的小量组织样品与高密度的锆珠放入可密封的2ml螺旋盖微量管中,再加入缓冲液与稳定成份到1.5ml的体积,用6500RPM振荡机高速上下振动8秒,休息8秒,再振动8秒即可。
此方法是目前最快且一次可处理最多样品的方法。
2、物理方法
反复冻融法:
破坏细胞膜的疏水键、溶胀
细胞--------融解--------融解…
超声波处理:
超声波的机械振动破碎细胞方法简单,重复性好
3、化生法
自溶法:
特定ph和温度下,细胞自溶,时间长,需要防止细胞污染
酶溶法:
溶菌酶、纤维素酶、蜗牛酶、蛋白酶、甘露糖酶、脂酶…细胞壁、细胞膜--生物酶-细胞溶解控制温度、酸碱度、酶用量、先后次序、时间,加入巯基试剂、尿素能增加效果
✧溶菌酶:
要通过破坏细胞壁中的N-乙酰胞壁酸和N-乙酰氨基葡糖之间的β-1,4糖苷键,使细胞壁不溶性黏多糖分解成可溶性糖肽,导致细胞壁破裂内容物逸出而使细菌溶解。
✧蜗牛酶:
从蜗牛的嗦囊和消化道中制备的混合酶,它含有纤维素酶,果胶酶,淀粉酶,蛋白酶等20多种酶。
✧纤维素酶:
葡聚糖内切酶、葡聚糖外切酶和β-葡萄糖糖苷酶三个主要成分组成的复合酶系。
✧半纤维素酶:
木聚糖酶、甘露聚糖酶、阿拉伯聚糖酶、阿拉伯半乳糖酶和木葡聚糖酶等多组酶的总称。
✧脂酶:
一种催化脂类的酯键水解反应的水溶性酶。
脂酶是酯酶下的一个亚类。
4、化学渗透法
有机溶剂、表面活性剂、金属螯合剂、变性剂-改变-细胞壁或膜的通透性--释放---内容物
细胞破碎方法
组织种类
细胞破碎方法
组织种类
旋刀式匀浆
动植物组织
酶溶
细菌、酵母
手动式匀浆
动物组织
去垢剂渗透
组织培养细胞
超声
细胞悬浮液
有机溶解渗透
细菌、酵母
高速匀浆
细菌、酵母、植物细胞
低渗裂解
红细胞、细菌
研磨
细菌、植物细胞
冻融裂解
培养细胞
高速珠磨
细胞悬浮液
二、蛋白质的抽提:
(选择合适缓冲液把蛋白质提取出来注意温度,防蛋白变性、降解(加入蛋白酶抑制剂)将蛋白质与非蛋白质分离,将各种不同的蛋白质分离。
1.沉淀法
(1)盐析法
中性盐对蛋白质的溶解度有显著影响;蛋白稳定因素:
水化膜,电荷。
蛋白质在低盐浓度下溶解度随盐浓度的增高而上升(盐溶),当盐浓度升高到一定程度时,其溶解度呈现不同程度下降,并不断析出(盐析)。
盐析是由于,盐浓度增高到一定数值,使水合作用降低,进而导致蛋白质分子表面电荷逐渐被中和,水化膜被破坏,蛋白质分子之间相互聚集并从溶液中析出。
盐溶:
在低盐浓度下随着盐浓度升高,蛋白质的溶解度增加。
盐析:
盐浓度比较高,随着盐浓度升高,蛋白质的溶解不同程度下降并先后析出
离子强度对盐析过程的影响
Cohn经验公式:
S--蛋白质溶解度,mol/L,I--离子强度;
Β--盐浓度为0时,蛋白质溶解度的对数值。
与蛋白质种类、温度、pH值有关,与盐无关;
Ks--盐析常数,与蛋白质和无机盐的种类有关,与温度、pH值无关。
✧Ks盐析法:
在一定pH和温度下,改变体系离子强度进行盐析的方法;
✧β盐析法:
在一定离子强度下,改变pH和温度进行盐析;由于溶质溶解度变化缓慢,且变化幅度小,因此分辨率更高,常用于初步的纯化。
✧Ks盐析法:
由于蛋白质对离子强度的变化非常敏感,易产生共沉淀现象,因此常用于提取液的前处理。
△盐析用盐的选择:
半径小的高价离子盐析作用较强;半径大的低价离子盐析作用较弱。
(Ks)磷酸钾>硫酸钠>硫酸铵>柠檬酸钠>硫酸镁
常用的盐析用盐:
硫酸铵:
溶解度大(767g/L)、硫酸钠、磷酸盐、柠檬酸盐
△影响盐析的因素
1 溶质种类的影响:
Ks和β值
2 溶质浓度的影响:
浓度大,盐的用量小,共沉作用明显,分辨率低;
3 pH值:
影响蛋白质表面净电荷的数量,通常调整体系pH值,使其在pI附近;
4 盐析温度:
大多数情况下,高盐浓度下,温度↑,蛋白质溶解度↓;
(2)有机溶剂沉淀法
蛋白质在一定浓度的有机溶剂的溶解度差异而分离
△优点:
分辨能力比盐析法高;
沉淀不用脱盐;
生化制备应用比较广泛
△缺点:
容易使蛋白活性丧失,操作温度低
有机溶剂的选择:
能和水混溶:
乙醇、甲醇、丙酮、DMSO…
△有机溶剂沉淀法的影响因素
1 温度:
低温降低溶解度,保持蛋白活性
2 样品浓度和ph:
样品浓度高,共沉淀高,等电点时蛋白溶解度最小
3 金属离子:
多价阳离子降低蛋白质溶解度,不影响其活性,盐浓度不能过高<5%,使用乙醇不超过2倍体积
(3)等电点沉淀法
不同的蛋白质有不同的等电点,位于等电点时,溶解度最低,
蛋白质与金属离子结合,等电点会偏移。
等电点方法多与其他方法联合使用,注意要制备的蛋白质对酸碱的稳定性,活性的影响
(4)生成盐复合物沉淀法
金属复合盐法:
蛋白质在碱性溶液中带负电,能与金属离子形成沉淀。
蛋白质-金属离子复合物对溶液的介电常数敏感。
有机盐法:
含氮有机酸如苦味酸、苦酮酸、鞣酸等能如蛋白质分子的碱性集团形成复合物沉淀析出。
容易发生不可逆反应,反应条件温和,加入稳定剂。
无机复合盐法:
无机盐如磷钼酸盐,磷钨酸盐等与蛋白形成复合物的溶解度低,极易沉淀析出。
常发生不可逆的沉淀反应,使蛋白变性。
(5)选择性变性沉淀法
利用蛋白质、酶和核酸等生物大分子对物理或化学因素敏感的差异,有选择地使之变性,以达到分离的目的。
可利用的因素有:
5 表面活性剂或有机溶剂(如三氯乙酸)
6 温度
7 酸碱变性…
(6)非离子多聚物沉淀法
溶液-除去-大颗粒-调整-ph、温度-加入-中性盐和多聚物-冷储-沉淀
非离子聚合物如聚乙二醇(PEG),壬基酚聚氧乙烯醚(NPEO),葡聚糖,右旋糖酐硫酸钠…
PEG:
原理:
PEG在溶液中形成了网状结构,与溶液中蛋白质分子发生空间排斥作用,使蛋白质分子凝聚、沉淀。
蛋白质的分子量越大,所需的PEG浓度越低;ph越接近等电点,所需的PEG浓度越低。
(7)免疫共沉淀:
将某一纯化蛋白质免疫动物可获得抗该蛋白的特异抗体。
利用特异抗体识别相应的抗原蛋白,并形成抗原抗体复合物的性质,可从蛋白质混合溶液中分离获得抗原蛋白。
(8)聚沉:
在聚沉剂的作用下,使胶体的微粒相互聚集为较大的聚沉物。
原理是:
①中和胶粒的电荷、②加快其胶粒的热运动以增加胶粒的结合机会,使胶粒聚集而沉淀下来。
聚沉剂主要是无机盐类(氯化锌,氯化铁…)和聚合无机盐(聚氯化铝、聚氯化铁…)
方法:
✓加入电解质,增加了胶体中离子的总浓度,而给带电荷的胶体粒子创造了吸引相反电荷离子的有利条件,从而减少或中和原来胶粒所带电荷,使它们失去了保持稳定的因素。
如:
豆浆做豆腐时,在一定温度下,加入CaSO4(或其他电解质溶液),豆浆中的胶体粒子带的电荷被中和,其中的粒子很快聚集而形成胶冻状的豆腐(称为凝胶)
✓加入带相反电荷的胶体,也可以起到和加入电解质同样的作用,使胶体聚沉。
如把Fe(OH)3胶体加入硅酸胶体中,两种胶体均会发生凝聚。
✓加热胶体,能量升高,胶粒运动加剧,它们之间碰撞机会增多,而使胶核对离子的吸附作用减弱,即减弱胶体的稳定因素,导致胶体凝聚。
如长时间加热时,Fe(OH)3胶体就发生凝聚而出现红褐色沉淀。
(9)絮凝
在絮凝剂的作用下,将不稳定颗粒诱导结合到一起,逐渐紧密,随后形成更大的凝聚物。
聚沉剂有淀粉、树脂、单宁、离子交换树脂和纤维素衍生物。
无机絮凝剂主要是依靠中和粒子上的电荷而凝聚,故常常被称为凝聚剂。
絮凝原理可分为化学絮凝和物理絮凝两种。
化学絮凝:
加入絮凝剂后由于彼此的化学反应造成胶质粒子的不稳定状态。
物理絮凝:
加入与胶体粒子具有不同电性的离子溶液时,会发生凝结作用,中和电性,不稳定的胶体粒子再互相碰撞而形成较大的颗粒。
碰撞后粒子便经由不同的物理化学作用而开始凝集,较大颗粒粒子从水中分离而沉降。
2.透析法
利用透析袋把大分子蛋白质与小分子化合物分开的方法。
可以除盐、除少量有机溶剂、除去生物小分子杂质和浓缩样品。
透析平衡需要的时间比较长,耗时。
透析膜可能含有极微量
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 蛋白质 工程
 冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《赶海》的教学设计.docx
《赶海》的教学设计.docx
