 高中化学奥赛培训教程全集---之有机化学Word下载.doc
高中化学奥赛培训教程全集---之有机化学Word下载.doc
- 文档编号:8047858
- 上传时间:2023-05-09
- 格式:DOC
- 页数:47
- 大小:914.50KB
高中化学奥赛培训教程全集---之有机化学Word下载.doc
《高中化学奥赛培训教程全集---之有机化学Word下载.doc》由会员分享,可在线阅读,更多相关《高中化学奥赛培训教程全集---之有机化学Word下载.doc(47页珍藏版)》请在冰点文库上搜索。
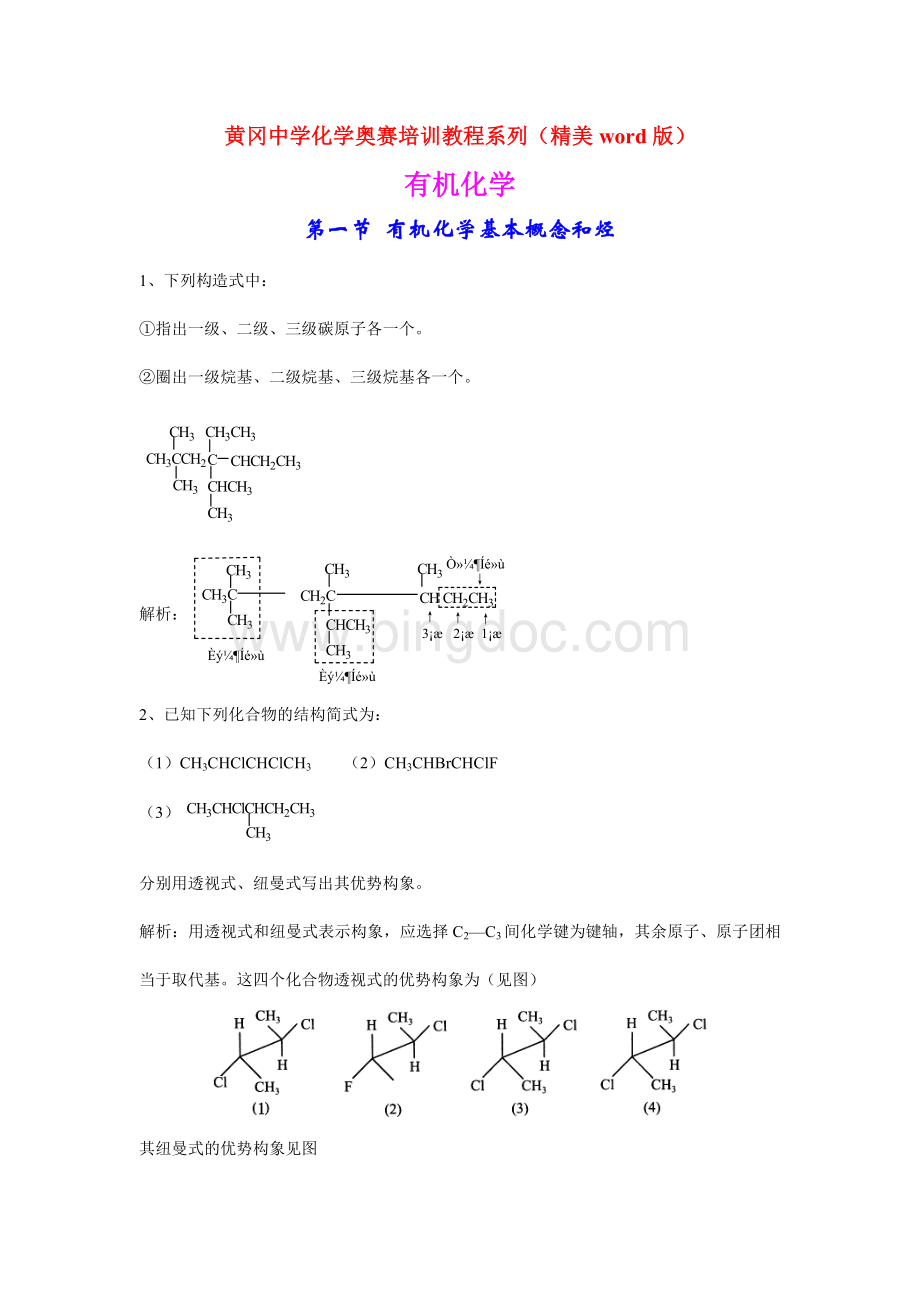
8、命名下例脂环烃。
(I)是螺环烃,名称为5-乙基螺[2·
4]庚烷,(II)的名称为6-甲基双环[3·
2·
2]壬烷,(III)的名称为8,8-二甲基双环[3·
1]辛烷,(IV)的名称为双环[2·
2]—2,5,7-辛三烷。
9、写出下列化合物的一对构象异构体,指出哪一个是优势构象。
(1)取代基在1,3位是一个反式结构应有两种构象(如下图)两个基团,一个处于a键另一个处于e键,由于大基团处于e键较稳定,所以两种构象中a为优势构象。
(2)取代基在环的1,4位,也是反式结构,也有两种构象,a式中基团均在a键,b式中基团均在e键,所以b式为优势构象。
(3)取代基在环的1,3位,是顺式异构体,在a式与b式两种构象中,b式为优势构象。
10、将下列各组化合物按取代反应由易到难顺序排列。
(1)组中,甲苯的苯环由于甲基的斥电子效应,电子云密度比普通苯环大,所以更易取代。
硝基是强吸电子在,可降低苯环电子云密度,使苯环难于取代,硝基越多取代越难,所以顺序为
(2)第一类定位基定位效应越强,苯环电子云密度越大越易取代,第二类定位基定位效应越强苯环电子云密度越小,越难取代。
所以顺序为
11、将下列化合物硝化,试用箭头表示硝基进入的位置(指主产物)。
12、在沥青的气体中存有稠环芳烃,其中一些可视为萘(A)、芘(B)、蒽并蒽(C)的同系物,同样,原子增加还可以有D、E等。
(1)试推测该系列化合物中,碳的最大质量分数。
(2)A+H2反应可能有多少种产物生成?
它们之中哪一种是热力学最稳定的?
(3)设氢化反应在相邻的位置上进行,试推测在B+2H2的反应中,哪种产物最稳定?
(1)可从A、B、C的分子式入手。
A、B、C的分子式分别为C10H8、C16、H10、C22H12。
按A、B、C的顺序递增C6H2,所以,该系列化合物的分子式可表示为:
C10H8+(C6H2)n,n为正整数,当n趋向无穷大时,化合物的含碳量最高。
即:
(2)A为大的共轭体系。
十个位置中(如图所示),每个位置都可加上一个氢原子,当A与1moLH2加成时,两个氢原子似乎可加到十个位置的任意两个位置上,但要注意,加上1molH2后,还有4个双键,必须满足碳原子间能构成4个双键,但不能1、3加成,因为在1、3位加上一个氢原子后,1、3碳上都形成了四个键,而碳2上只形成了三个键,又无法跟邻近的碳原子构成双键,故不能有这种加成方法。
由于可加成的位置比较多,必须按一定顺序进行,否则容易出现漏写和重写。
同时须注意,A是一个对称结构,存在x、y两根对称轴,处于对称位置上的双键,加成后得到相同的产物。
如1、2加成与6、7加成,2、3加成与7、6加成都会得到相同的产物。
可先写出连位加氢的结构,连拉加氢有1、2,2、3,9、10,1、9四种加法,须注意共轭体系中双键的转移,其产物结构分别为:
再写不连位加氢的结构,不连位加氢有1、4,1、5,1、7,2、6,2、10五种加法,其结构分别如下:
另外,还可这样考虑,加成1molH2后,破坏了原A的共轭结构,加两个氢原子后,由于有多种加法,就可能形成多种产物,有多少种加法,就会生成多少种产物。
反之,有多少种产物,则有多少种加法。
能否直接判断有多少种产物?
是可以的。
即为产物在结构中形成四个双键,只需写出其所有的同分异构体,即可知道产物有多少种。
我们可按一定的顺序来书写同分异构体。
①保持一个苯环结构,加成1molH2的结构有两种:
②保持一个苯环中两个双键不动的加成法有四种:
③原来结构全部被破坏的有三种:
当然还有多种其他的分类方法,都可顺利地写出九种异构体。
在九种产物中,热力学最稳定的产物是哪一种呢?
考虑稳定性,可从双键的共轭情况入手,整个体系共轭得越好,结构就越稳定,同时注意,苯环是非常稳定的特殊共轭体系。
九种异构体中,含有苯环的有两种,四个双键全处于共轭状态的有五种,当然是既含有苯环又使四个双键全部处于共轭状态的结构最稳定。
所以,最稳定的结构为:
(3)B分子结构中,共含有八个双键,加成2molH2后,还剩六个双键,六个双键构成两个苯环结构时,结构最稳定。
结构式如下:
答案:
(1)该系列化合物中,碳的最大质量分数为:
(2)A+H2反应可能有九种产物生成,热力学最稳定的异构体为:
(3)最稳定的产物是:
第二节烃的衍生物
1、某一溴代烷A1.37克在干燥乙醚中与镁作用,然后加入水,结果产生0.58克气态烃B。
A溴代可生成三种二溴代物同分异构体,求A、B结构简式。
设分子式CnH2n+1Br,据题意
CnH2n+1BrCnH2n+1MgBrCnH2n+2
14n+8114n
1.370.58
(14n+81)︰1.37=14n︰0.58n=4
因为A能生成三种二溴代物,故A为(CH3)2CHCH2Br,B为(CH3)2CHCH3。
2、(2005年江苏集训题)用化学方法区别下列各组化合物:
(1)1—溴—1—戊烯、3—溴—1—戊烯和4—溴—1—戊烯。
(2)对氯甲苯、氯化苄和β—氯乙苯。
(1)用AgNO3乙醇溶液。
1—溴—1—戊烯是乙烯式卤代烃,与AgNO3溶液不反应,3—溴—1—戊烯是烯丙式卤代烃与AgNO3溶液立即生成淡黄色沉淀,4—溴—1—戊烯是孤立式卤代烯烃,性质与卤烷相似,需加热后才生成沉淀。
(2)用AgNO3乙醇溶液。
氯化苄立即生成白色沉淀,对氯甲苯不反应,β—氯乙苯加热后生成白色沉淀。
3、(2005年河南省集训题)以1—碘丙烷制取下列物质。
(1)异丙醇。
(2)α-溴丙烯。
(3)1,3—二氯—2—丙醇。
(4)2,3一二氯丙醇。
(1)CH3CH2CH2ICH3CH=CH2
(2)CH3 CH2CH2ICH3CH=CH 2CH2BrCH=CH2
(3)CH 3CH2CH2ICH3CH=CH2CH2ClCH=CH2
CH2ClCHOHCH2Cl
(4)CH3CH2CH2ICH3CH=CH2
CH2OHCH=CH2CH2OHCHClCH2Cl
4、(2005年山东省集训题)用化学方法区别下列化合物:
(1)乙醇、2-丙醇、2-甲基-2-丙醇,
(2)乙醇、乙醚、氯乙烷。
(1)用卢卡斯试剂,2-甲基-2-丙醇立即变浑浊,2-丙醇数分钟后党浊,乙醇无现象。
(2)能与金属钠反应生成气体的为乙醇,余下的能溶于浓硫酸的是乙醚,无现象为氯乙烷。
5、(2005年山东省集训题)化合物A的分子式为C5H11Br,和NaOH溶液共热后生成C5H12O(B),B具有旋光性,可和钠反应生成H 2,B和浓硫酸生成C5H10(C),臭氧化后得丙酮和乙醛,写出A、B、C结构简式。
可采用逆推方式,从臭氧化产物可知C是。
在几步反应中碳链未变,所以A为B为
6、(2001年山西省集训题)以乙烯和2-丙醇为原料合成3—甲基—1-丁醇。
CH2=CH2+
(CH 3)2CHOH(CH3)2CHBr(CH3)2CHMgBr
(CH3)2CHCH2CH2OMgX(CH3)2CHCH2CH2OH
7、以化学方法鉴别下列化合物:
乙苯,苯乙醚,对—乙基苯酚,1—苯基乙醇。
先用NaOH溶液,能溶解于NaOH溶液的是对—乙基苯酚,加入金属钠有气体生成的是1—苯基乙醇。
也可用卢卡斯试剂,数分钟后有浑浊,能溶于浓酸的是苯乙醚,剩余的为乙苯。
8、下列化合中,哪些可形成分子内氢键?
哪些可形成分子间氢键?
(1)对苯二酚。
(2)邻苯二酚。
(3)邻甲苯酚。
(4)邻氟苯酚。
能形成分子内氢键的为邻苯二酚和邻氟苯酚。
对苯二酚两个羟基位置较远,不能形成分子内氢键,只可形成分子间氢键。
邻甲苯酚的甲基无形成氢键能力,只能形成分子间氢键。
9、(2005年黄冈中学培训题)以苯为主要原料制取苯甲醚。
以苯为主要原料制取
10、用简便方法鉴别下列化合物:
(1)3—戊醇。
(2)2—戊酮。
(3)戊醛。
(4)3—戊酮。
(5)苯甲醇。
(6)2—戊醇。
(2)、(3)、(4)、(5)可与2,4-二硝基苯肼生成有色苯腙,其中(3)、(5)可与多伦试剂生成银镜,而(5)不能与斐林试剂反应。
在
(2)和(4)中,
(2)可发生碘仿反应,(4)不是甲基酮不能反应。
(1)和(6)中,(6)可与I2+NaOH发生碘仿反应。
11、(2005年黄冈中学强化题)以苯为原料和必要的无机试剂合成己二醛。
12、化合物A(C5H12O)有旋光性,它在碱性KMnO4溶液作用下生成B(C5H10O),B无旋光性。
B与正丙基溴化镁反应,水解后得C,C经拆分可得互为镜象的两个异构体,推测A、B、C的结构。
A从组成和题意可知为醇。
碳五的醇有光学活性的只有2—戊醇和3—甲基—2—丁醇,氧化后成酮。
2—戊醇氧化后的酮与正丙基溴化镁反应不可能有光学活性物质生成(2—戊酮羰基碳上有两个正丙基),所以A只可能是3—甲基—2—丁醇。
反应为:
13、比较下列各物质酸性的强弱。
(1)C6H5OH。
(2)CH3COOH。
(3)F3CCOOH。
(4)ClCH2COOH。
(5)C2H5OH。
卤代酸由于诱导效应,酸性强于羧酸,卤原子多酸性更强。
所以酸性从强到弱顺序为:
F3CCOOH>
ClCH 2COOH>
CH3 COOH>
C6H5OH>
C2H5OH。
14、(2005年黄冈中学强化训练题)用化学方法区别下列各组化合物。
(1)甲酸、乙酸、丙二酸。
(1)取样品加热,有气体生成且可使石灰水浑浊的是丙二酸,剩余两种,中和后可与多伦试剂反应生成银镜的为甲酸,还有一种则为乙酸。
(2)能与FeCl3溶液显色的是邻羟基苯甲酸,能与NaHCO3溶液生成气体的为苯甲酸,还有一种为苯甲醇。
15、试以乙醇为原料合成丁酸。
16、用化学方法区别下列化合物:
(1)乙酰氯。
(2)乙酸酐。
(3)氯乙烷。
加水后与水不发生反应的为氯乙烷;
加水后滴入AgNO 3溶液有白色沉淀的是氯乙酸;
加水后是酸性,但不能和AgNO3溶液生成白色沉淀的是乙酸酐。
17、用丙二酸酯法合成己二酸。
丙二酸二乙酯为原料合成羧酸,它本身最后只剩下两个碳原子,其中一个是羧基,要得到二元酸则必需用两分子丙二醇二乙酯和二元卤代烃作用才行,所以可用1,2—二溴乙烷。
18、由乙醇为原料合成3—甲基—2—戊酮。
3—甲基—2—戊酮是一个甲基酮,故可用乙酰乙酸乙酯法来合成,因为本题未允许用其他有机物,所以除无机原料和催化剂外,所用有机试剂均需自己制备。
C2H5OHCH3COOHCH3COOC2H5
2C2H5OH+2Na2C2H5ONa+H2↑
C2H5OH+SOCl2C2H5Cl+SO2+HCl
C2H5OHC2H42HCHOCH3OHCH3Br
CH3COOC 2H5CH2(COOC2 H5)2CH3COCH2COOC2H5
19、比较下列各组化合物的碱性。
(1)苯胺、乙胺、二乙胺、二苯胺。
(1)胺的碱性为脂肪促胺强于伯胺、强于芳胺,所以碱性从强到弱的顺序为二乙胺>
乙胺>
苯胺>
二苯胺。
(2)芳胺芳环上若有斥电子基可增强碱性,若有吸电子基则减弱碱性,所以碱性从强到弱顺序为:
20、下列化合物如何提纯?
三乙胺中含少量乙胺和二乙胺。
三乙胺为叔胺,杂质为伯胺和仲胺,可先加入足量乙酰氯,乙胺和二乙胺生成酰化物,三乙胺氮原子上无氢不反应,加入盐酸和三乙胺生成盐酸盐,用乙醚提取酰化物,分液后,将盐酸盐用碱中和再蒸馏即得三乙胺。
21、用R—S法标记下列化合物中的手性碳原子的构型。
(1)先变成费歇尔投影式。
(2)投影式为:
(3)先变换成透视式,再变换成投影式。
22、用“*”标出下列化合物中手性碳原子,有顺反异构时写出其顺、反异构体并命名。
(1)CH2BrCHDCH2Cl
(2)HOOCCHOHCOOH
(3)(4)CH3CHOHCH2CH3
(1)H与D是不同的氢原子,所以C2是手性碳原子。
CH2BrCHDCH2Cl。
(2)分子对称,无手性碳原子。
(4)C2为手性碳原子。
23、写出分子式为C3H6BrCl的所有异构体的结构简式,用“*”号标出手性碳原子,用投影式表示各对映体,并指出R—S构型。
(I),CH3CBrClCH3,CH2BrCH2CH2Cl。
24、写出β-D(+)半乳糖的哈武斯式(吡喃型)。
25、用化学方法区别下列化合物。
(1)葡萄糖和葡萄糖酸。
(2)葡萄糖酸和葡萄糖醇。
(1)葡萄糖分子中含醛基可与多伦试剂生成很镜,葡萄糖酸无现象。
(2)将两样品分别加入滴有酚酞的NaOH溶液能使红色褪去的为葡萄糖酸。
26、在测定糖结构时,常用溴水将糖氧化成酸,然后脱羧再将C2氧化成醛基,反复此过程可将乙醛糖依次变为戊醛糖、丁醛糖……。
已知L—乙醛糖A用溴水氧化可得光活性产物。
A递降得成戊醛糖B,B用NaBH4还原后,产物无光活性。
将B与HCN反应后用酸水解,再用锌汞齐在酸性条件下处理得A和另一异构体C,C用HNO3氧化,得无光活性的二酸,写出A、B、C的投影式。
L—己醛糖C5和C6为,戊醛糖用NaBH4反应,醛基还原成羟基成为糖醇,产物无光活性,所以分子有对称面,所以B的投影式为
27、用化学方法区别下列化合物。
(1)葡萄糖、蔗糖和淀粉。
(2)蔗糖、淀粉和纤维素。
(1)葡萄糖是还原糖,可与银氨溶液反应生成银镜。
淀粉可与碘水作用生成蓝色,还有一种为蔗糖。
(2)先用碘水鉴别出淀粉,其余二种分别在试管内加入几毫升稀硫酸加热数分钟,中和后用斐林试剂检验,有红色沉淀为蔗糖。
因为二糖易水解,纤维素不易水解,此条件下纤维素水解极弱可忽略。
28、(2005年黄冈中学强化题)化合物X是一种天然产物,化学式量为180。
1.98克X燃烧可生成1478.4mL的CO2(标),和1.188克的水,X可发生银镜反应,它与乙酸酐反应生成A,A的式量比X大116.67%,求X和A的结构简式。
先求X最简式,1.98克样品中,
碳原子为:
氢原子为:
氧原子为:
1.98-0.792-0.132=1.056(克)(即0.066mol)
C/H/O=0.066/0.132/0.066=1/2/1
化学式为(CH2O)n,
化学式为C6 H12O6。
A的式量为:
180×
216.67%=390。
X为:
CH2OH(CHOH)4CHO。
A为:
29、柳树皮中有一种糖苷叫水扬苷,用酶水解时,得D-葡萄糖和水杨醇(邻羟基苯甲醇)。
水杨苷用硫酸二甲酯和NaOH处理得五甲基水杨苷,酸水解得2,3,4,6-四甲基-D-葡萄糖和邻甲氧基苯甲醇。
写出水杨苷哈武斯式。
据题意,水杨苷中葡萄糖C1和C5 形成氧环,C1苷羟基本原则与水杨醇成苷,所以葡萄糖C2、C3、C4 、C6上羟基可甲基化,水杨醇上酚羟基也甲基化,所以哈武斯式为:
30、完成下列反应:
(1)甘氨酸盐酸盐+SOCl2。
(2)丙氨酸+HCl+NaNO2。
(3)丙氨酸
31、某二肽水解产物为甘氨酸和苯丙氨酸,写出其可能结构。
该二肽有两种可能结构:
32、橡胶工业所用的橡胶制品的粘合剂是将天然橡胶(聚异戊二烯)溶于汽油而制得,但硫化后的橡胶制品在汽油中只出现溶胀现象(不溶解,而体积膨胀),为什么?
天然橡胶即聚异戊二烯是一个线型高聚物,所以可以溶解于有机溶剂,由于天然橡胶的玻璃化温度不很低,所以温度稍低就发脆。
而粘流化温度又不太高,天气稍热就发粘,故性能不好,通常需硫化。
硫化时打开了聚异戊二烯的部分双键,高分子链间通过硫原子连结交联变成网状结构,所以在性能改善的同时,溶剂只发生溶胀而不溶解。
33、合成聚苯乙烯时,用含同位素标记的偶氮二异丁腈作引发剂,发现生成的聚苯乙烯分子带有两个引发剂分解时的碎片,问怎样的终止反应才能得到这种分子?
发生的是双基结合终止反应。
34、写出聚己内酰胺(锦纶-6,耐磨性最好的合成纤维)合成反应的历程(不必写副反应,链终止控制分子量常用醋酸)。
缩聚反应常用酸或碱作反应催化剂。
35、薄荷是一种香料,结构为,它具有特殊的薄荷香气,且口含时有凉爽之感,广泛用于化妆品工业、食品工业和医药工业中。
该结构有立体异构体;
异构体之间在香气强度、类型和凉爽作用上存在差别。
因此,对其异构体的研究在理论和实践上均有重要意义。
(1)用构型式表示具有上述结构的所有可能的立体异构体的构型。
(2)这些构型式中哪些互为对映体?
写出这些异构体中右旋体、左旋体、外消旋体和内消旋体的数目。
(3)写出各个构型式中手性碳原子的R、S构型。
(4)选用船型或椅型构象式表示各个顺反异构体的稳定构象。
(5)在第(4)你所写出的构象中,最稳定的是哪一个?
它的脱水反应产物是单一产物还是混合物?
试用构象式说明这个变化过程(产物不要求写出构象式,只写出结构式即可)。
(1)薄荷醇有3个手性碳原子,有8种(23)立体异构体。
(2)有4对对映体(实物有镜像不能完全重叠的2个立方体异构体,互为对映异构体)。
每对对映体中,有1个左旋体,1个右旋体;
等量左旋体和右旋体混合就组成外消旋体。
如分子内含有相同的手性碳原子,分子的两个半部互为物体和镜像关系,即为内消旋体。
(3)标记构型的方法可用R、S来标识,根据“次序规则”比较与手性碳原子相连的4个基团的大小进行判断。
(4)在构象异构体中,通常椅式比船式稳定,而在椅式构象中,e-取代基最多的构象为稳定构象。
有不同的取代基时,大的取代基在e键的构象最稳定。
在椅式构象中发生消去反应时,一般是处在反式共平面(a、a键)的两个基团易被消去,故最稳定构象的脱水反应产物是单一的。
(1)8种立体异构体的构型式:
(2)互为对映体的是①和②、③和④、⑤和⑥、⑦和⑧。
其中4个为左旋体,4个为右旋体,4个为外消旋体,无内消旋体。
(3)以羟基、异丙基、甲基的顺序的R、S构型如下:
①SRS②RSR③SRR④RSS⑤RRS⑥SSR⑦RRR⑧SSS
(4)稳定构象式:
(5)上述(4)中的第一个构象最稳定。
第三节反应机理有机推断与合成
1、有机物X可以还原生成醇,也可以氧化生成一元羧酸,该醇与该一元羧酸反应可生成分子式为C2H4O2的有机物,则下列五个结论中不正确的是()
A.X具有还原性
B.X由3种元素组成
C.X的相对分子质量为30
D.X中含碳的质量分数为40%
因醇与羧酸反应生成酯,故分子式为C2H4 O2的有机物的结构式为。
由此可判断X应是甲醛,它具有还原性,由3种元素组成,相对分子质量为30,含碳的质量分数为40%;
但分子结构中无甲基。
本题答案为C。
2、某有机物8.8g,完全燃烧后得到CO222.0g,H2O10.8g。
该有机物可能是()
由题目给出的条件,经计算每摩尔有机物完全燃烧应生成5molCO2和6molH2O,那么有机物的摩尔质量为88g·
mol-1,从而计算出该有机物的分子式为C5H12O。
故答案选B、C。
3、今有NaOH溶液、NaHCO3溶液、CH3COOH、C2H5OH四种试剂。
下列有机物在一定条件下能分别跟这四种试剂发生反应的是()
有机物分子中含有—COOH才可以与NaOH溶液、NaHCO3溶液和C2H5OH反应;
含有醇羟基才能与CH3COOH发生酯化反应。
答案为D。
4、将含有一种杂质(其质量小于0.3g)的丙醛试样8g与足量的银氨溶液反应,析出银30.6g,则该杂质可能是()
A.甲醛B.乙醛C.丁醛D.戊醛
设含杂质的醛的相对分子质量为M,其质量为mg。
因为
所以
当m<
0.3g时,代入得M<
33.6,应为甲醛。
答案选A。
5、下列化合物中,有顺、反异构体的是()
A.C6H5CH=CH2B.C6H5—NH—OH
C.C6H5CH=N—OHD.C6H5—NH—NH2
由于π键是镜面反对称,所以双键的上、下方不同基团的互换,就成了顺、反异构体。
B、D分子中,除了苯环外,不存在双键,所以没有顺、反异构体。
由于A分子中面端是两个H原子,不可能产生不同基团的互换,故应选C。
即
6、已知,卤代烃在碱性条件下可发生下列两类反应:
RCH2CH2X+H2ORCH2CH2OH+X-
RCH2CH2X+OH-RCH=CH2+X-H2O
早在1874年就合成了有机物DDT,1944年后广泛用作杀虫剂,后因具有高残毒被禁止使用。
若氯苯和苯酚具有相似的化学性质,则DDT可由氯苯和CCl3CHO相互反应制得。
DDT的化学式为C14H9Cl5。
(1)DDT的结构式_________,制备DDT的化学反应方程式为_____________。
(2)DDT
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 培训 教程 全集 有机化学
 冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 二年级下册数学专项练习-应用题1.docx
二年级下册数学专项练习-应用题1.docx
 红色精美二十届三中全会提出的新概念新观点新论断.pptx
红色精美二十届三中全会提出的新概念新观点新论断.pptx
