 醇、酚、醚和羰基化合物-化学竞赛夏令营-江苏.ppt
醇、酚、醚和羰基化合物-化学竞赛夏令营-江苏.ppt
- 文档编号:18698221
- 上传时间:2023-09-23
- 格式:PPT
- 页数:76
- 大小:2.18MB
醇、酚、醚和羰基化合物-化学竞赛夏令营-江苏.ppt
《醇、酚、醚和羰基化合物-化学竞赛夏令营-江苏.ppt》由会员分享,可在线阅读,更多相关《醇、酚、醚和羰基化合物-化学竞赛夏令营-江苏.ppt(76页珍藏版)》请在冰点文库上搜索。
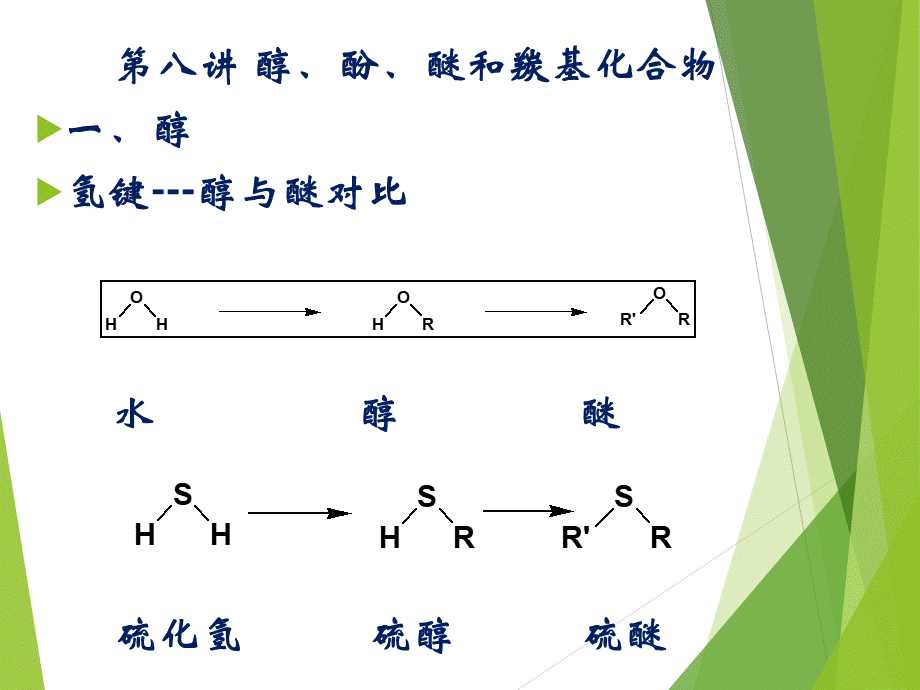
第八讲醇、酚、醚和羰基化合物一、醇氢键-醇与醚对比水醇醚硫化氢硫醇硫醚,醇分子间能形成氢键,醚分子中不含羟基分子间不能形成氢键,硫醇不能形成氢键,如:
CH3SH(M=48,bp=6)、CH3OH(M=32,bp=64.7);CH3CH2SH(M=62,bp=37)、CH3CH2OH(M=46,bp=78.3),维生素C分子结构中的烯二醇基C3位OH由于受共轭效应的影响,酸性较强(pKa=4.17);C2位OH由于形成分子内氢键,酸性极弱(pKa=11.75)。
故维生素C一般表现为一元酸,可与碳酸氢钠作用生成钠盐。
对羟基苯甲醛的分子间氢键,邻羟基苯甲醛的分子内氢键,BP:
196.5,BP:
246.6,对羟基苯甲醛的酸性大于苯酚邻羟基苯甲醛的酸性小于苯酚,分子中羟基越多形成的氢键越多,如:
Bp:
19712584,硫醇的酸性比醇强CH3CH2SH:
pka=10.5;CH3CH2OH:
pka=17,1.制备:
(1)烯烃的水合,(B)间接水合(a)加硫酸(遵循马氏),(A)直接水合(遵循马氏),(b)硼氢化-氧化(反马氏),
(2)卤代烃的水解(3)羰基化合物的还原,醛酮的还原:
催化加氢/Pd、Pt、Ni,,NaBH4(不还原碳碳双键、碳碳叁键、氰基、硝基),LiAlH4(不还原碳碳双键、碳碳叁键),羧酸、酯的还原:
催化加氢/Pd、Pt、NiLiAlH4乙硼烷还原羧酸羧酸很难用催化氢化法还原,一般转化为酯再还原,(4)格氏反应醛和酮与Grignard试剂(RMgX)发生加成反应,加成产物水解生成醇。
甲醛与RMgX反应用于合成伯醇;其它醛与RMgX反应用于合成仲醇;酮与RMgX反应用于合成叔醇。
酰卤、酯、酸酐与Grignard试剂(RMgX)发生加成-消去反应生成酮,进而再与RMgX反应生成叔醇。
低温酰卤、酸酐与RMgX反应可停留在酮阶段用于制备酮。
腈与RMgX反应生成酮,与活泼金属反应得到的醇金属盐一般用作强碱,与活性氢反应生成碳负离子作为亲核试剂进行取代或加成反应。
常用于酯-酯缩合,酮-酯缩合,迈克尔加成等。
3反应:
(1)与活泼金属的反应(Na、K、Al),对于氢活性较弱的可以用更强的碱,如氢化钠、氨基钠等.,
(2)与卤化氢的反应:
Lucas试剂,HX=HI,HBr,HCl活性依次减弱。
叔醇仲醇伯醇,Lucas试剂(浓盐酸/无水氯化锌),(3)与卤化磷和亚硫酰氯作用,(4)与无机酸成酯-硝酸甘油酯、硫酸氢甲酯和硫酸二甲酯,(4)脱水反应,扎依采夫规则:
脱去的是羟基和含氢较少的碳上的氢。
也有一些不符合扎依采夫规则,(5)氧化(KMnO4/H2SO4、Na2Cr2O7/H2SO4),(6)邻二醇的制备和氧化开裂,烯烃氧化制备1,2-二醇(顺式),环氧化合物水解制备1,2-二醇(反式)邻二醇的氧化开裂,二、酚1制备:
(1)磺化碱熔,
(2)芳卤的水解,2.反应:
(1)酚羟基上的反应,酸性(与醇对比)苯酚的pKa=10,它的酸性比醇强(乙醇的pKa=17;环己醇的pKa=18),比碳酸弱(pKa=6.38),与FeCl3的颜色反应(凡是具有烯醇式结构的脂肪族化合物都反应)与酰氯、酸酐成酯,
(2)与溴水反应三、醚1制备:
(1)醇分子间脱水(制备单醚),
(2)Williamson醚的制备,乙基叔丁基醚的制备:
酚醚的制备:
2反应:
(1)醚键的开裂,三溴化硼和三氯化铝等路易斯酸也能使醚键断裂,如:
合成上常用苄基醚保护羟基,再采用催化氢化还原脱保护。
(2)环氧乙烷的开裂:
酸催化开裂:
碱催化开裂:
不对称环氧化合物的开裂:
抗生素麦咪诺的合成,例题,一种含硅阻燃剂的合成,1制备:
(1)醇的氧化常用的氧化剂:
四、醛酮化合物,重铬酸钾/硫酸;高锰酸钾/硫酸。
只适应制备低级的挥发性高的醛(采用边滴加边蒸馏),高级醛会进一步氧化成羧酸;KMnO4一般不用于仲醇氧化成酮的制备,会发生碳链断裂。
Collins试剂(CrO3Py2),PDC(重铬酸Py2)或PCC(氯铬酸Py2)用于氧化伯醇至醛类的氧化剂,对于氧化仲醇至酮类同样适用;分子中如存在不饱和键不受影响。
Oppenauer氧化(丙酮-异丙醇铝)和Jones试剂(CrO3-H2SO4)不饱和仲醇用丙酮-异丙醇铝或Jones试剂为氧化剂,可得相应不饱和酮;Oppenauer氧化不适合伯醇,生成的醛在碱性条件下可自身或与丙酮发生羟醛缩合。
Jones试剂可将伯醇氧化为羧酸。
活性二氧化锰活性二氧化锰可以氧化不饱和伯、仲醇(烯丙醇或苄醇)为相应的不饱和醛、酮。
(2)炔烃的水合(3)傅克酰基化反应,3反应:
(1)亲核加成(HCN、NaHSO3、醇、格氏试剂、氨的衍生物)(A)与氢氰酸的加成反应脂肪族酮发生加成反应,生成羟基腈(即氰醇)由于HCN为弱酸,加入碱使其离解为CN-,从而加速反应。
氰醇中,氰基可以水解成羧基然后酯化,也可还原成氨基甲基,羟基可脱水和氨基化。
有机玻璃单体和噁唑烷酮可以此为原料合成。
有机玻璃单体:
-甲基丙烯酸甲酯,噁唑烷酮,(B)与亚硫酸氢钠的加成反应大多数醛和脂肪族甲基酮能与亚硫酸氢钠发生加成反应,生成羟基磺酸。
羟基磺酸易溶于水,但不溶于饱和的亚硫酸氢钠溶液,故可用于鉴别醛和酮。
(C)与醇的加成反应在无水HCl或其它无水强酸的催化下,醛(酮)与一分子醇反应生成半缩醛(半缩酮),进一步与一分子醇缩合生成缩醛(缩酮)。
由于缩醛(缩酮)对氧化剂和碱稳定,可以用来保护羰基,等反应结束后在酸的水溶液中加热水解去掉保护,重生羰基。
D)与Grignard试剂的加成反应醛和酮与Grignard试剂(RMgX)发生加成反应,加成产物水解生成醇。
甲醛与RMgX反应用于合成伯醇;其它醛与RMgX反应用于合成仲醇;酮与RMgX反应用于合成叔醇。
(E)与氨的衍生物加成反应醛和酮与氨的衍生物(羟胺、肼、2,4-二硝基苯肼、氨基脲)作用,分别生成肟、腙、2,4-二硝基苯腙、缩氨脲。
(2)氢的活泼性:
醛、酮与氨的衍生物的反应,除了合成意义外,常常用于羰基化合物的鉴别与分离。
因为反应后的生成物大部分是固体,且具有一定的熔点,可利用来鉴别醛、酮。
在稀酸作用下,又水解成原来的醛、酮,可利用来分离和提纯醛、酮.,(A)烯醇互变异构,(B)羟醛缩合反应在稀碱存在下,两分子醛(酮)相互作用,一分子的氢加到另一分子的羰基的氧原子上,而其余部分加到另一分子的羰基的碳原子上,生成羟基醛(酮),羟基醛(酮)受热生成,-不饱和醛(酮)。
含氢的两种醛(酮)之间的产物有四种在合成中没有意义;如果两者之一不含氢(如甲醛、苯甲醛、糠醛),则产物为两种,在合成中有着重要意义。
(C)醛(不含的氢醛)与硝基化合物的缩合,(D)酮与不含氢酯的缩合不含氢酯:
苯甲酸酯、甲酸酯、碳酸酯、草酸二酯等,(E)Mannich反应,(F)卤代及卤仿反应卤代反应:
p286.4.卤仿反应:
凡具有CH3CO-结构的醛、酮,或具有CH3CH(OH)-结构的醇能发生卤仿反应。
由于碘仿是不溶于水的黄色的固体,且具有特殊的气味,可用于鉴别。
(3)氧化还原反应(A)氧化反应醛易被氧化,可被弱的氧化剂Fehling试剂(以酒石酸盐为络合剂的碱性氢氧化铜)或Tollen试剂(硝酸银的氨溶液)氧化,而碳碳不饱和键双键不受影响。
RCHO+Cu(OH)2+NaOHRCOONa+Cu2ORCHO+Ag(NH3)OHRCOONH4+Ag酮不易被氧化,在强烈氧化条件下,发生碳碳键的氧化开裂,一般在合成上没有意义。
(B)还原反应(a)催化氢化,醛、酮在Ni、Cu、Pt、Pd等的催化作用下与氢反应生成醇。
(b)金属氢化物还原(c)Clemmenson还原醛和酮用锌汞齐加盐酸可还原为烃。
(d)Wolff-Kishner-黄鸣龙醛和酮与肼在高沸点溶剂如一缩二乙二醇中,首先与肼生成腙,腙在碱性条件下加热失去氮,羰基转变为亚甲基。
Clemmenson还原和Wolff-Kishner-黄鸣龙还原都可将羰基还原为亚甲基,前者在酸性性条件下进行,后者在强碱条件下进行,根据反应物分子中其它基团对反应条件的要求,选择使用。
(e)Cannizzro反应不含氢的醛在浓碱存在下,发生自身的氧化还原-歧化反应,一分子还原为醇,另一分子氧化为酸。
RCHO+浓NaOHRCOONa+RCH2OH(4)乙烯酮及双乙烯酮的反应制备:
练习题:
1他莫昔芬(Tamoxifen)是一种合成的非甾体类三苯乙烯衍生物,由帝国化学工业公司研究开发,具有抗雌激素和雌激素样双重作用,主要用于治疗乳腺癌,其合成的路线如下:
(1)写出A、B、C、D、E的结构式或化学式;
(2)写出的制备方法;(3)化合物G是否有顺反异构,并用Z/E法标出;(4)用*标出E、F的手性碳。
2桂利嗪是钙拮抗剂类周围血管扩张药,其合成路线如下:
(1)写出A、B、C、D、E、F、G的结构式;
(2)标出桂利嗪分子的手性碳,是否有顺反异构,并用Z/E法标出。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 羰基 化合物 化学 竞赛 夏令营 江苏
 冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 甲醇合成的仿真实验报告.docx
甲醇合成的仿真实验报告.docx
 建筑LEC危险源辨识清单.xls
建筑LEC危险源辨识清单.xls
