 .酶催化反应的动力学
.酶催化反应的动力学
- 文档编号:15992646
- 上传时间:2023-07-09
- 格式:DOC
- 页数:6
- 大小:98KB
.酶催化反应的动力学
《.酶催化反应的动力学》由会员分享,可在线阅读,更多相关《.酶催化反应的动力学(6页珍藏版)》请在冰点文库上搜索。
第三节酶催化反应的动力学
复习题问:
略
新授:
Ⅰ酶反应动力学的概念:
研究酶促反应速度及其影响因素(哪些因素影响、如何影响)称酶促反应动力学。
Ⅱ酶反应动力学的影响因素:
酶浓度、底物浓度、pH、温度、抑制剂及激活剂等。
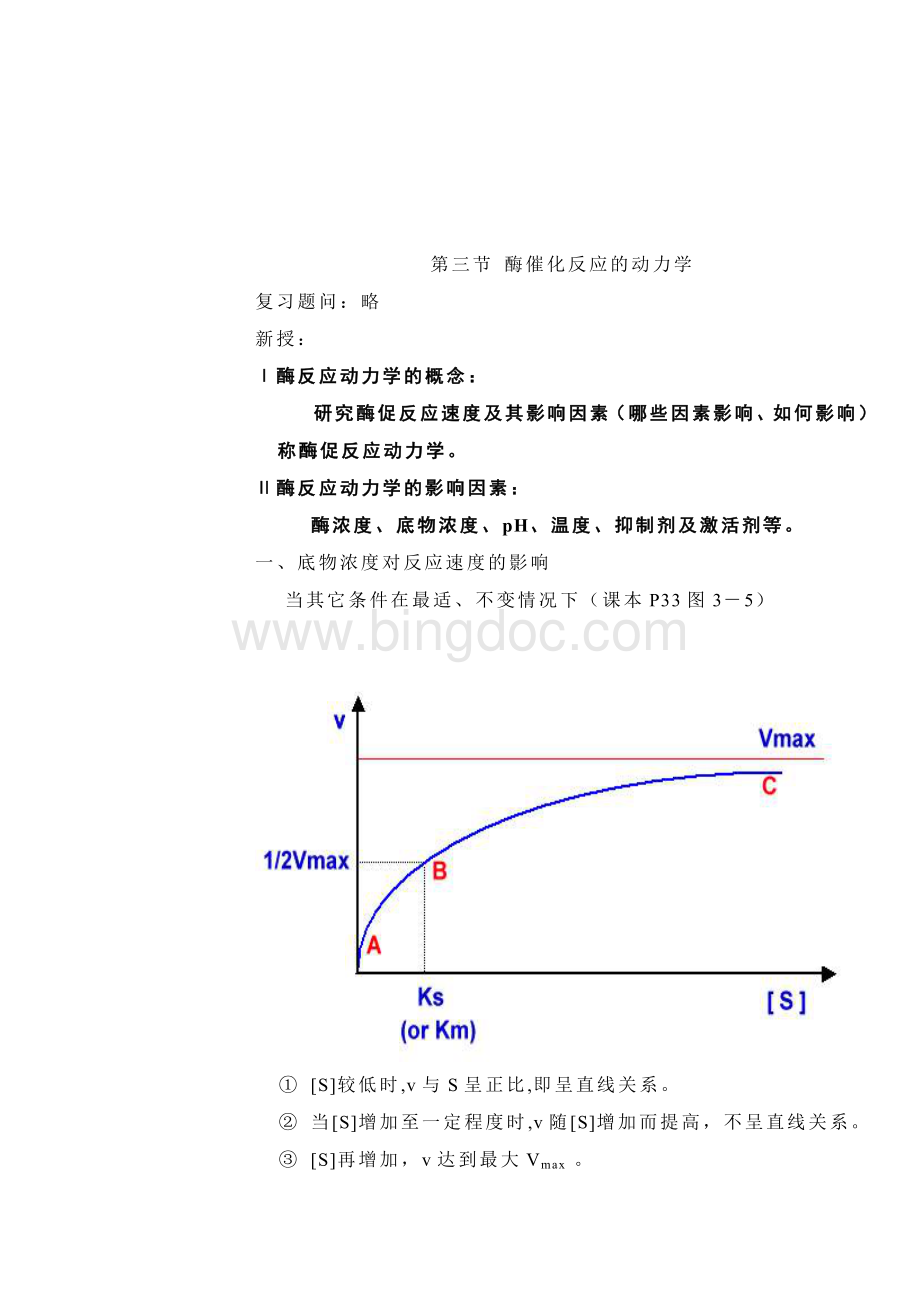
一、底物浓度对反应速度的影响
当其它条件在最适、不变情况下(课本P33图3-5)
①[S]较低时,v与S呈正比,即呈直线关系。
②当[S]增加至一定程度时,v随[S]增加而提高,不呈直线关系。
③[S]再增加,v达到最大Vmax。
(一)米-曼氏方程式:
⒈概念:
酶促反应速度与底物浓度关系的数学方程式。
⒉方程式:
说明:
⑴Vmax为最大反应速度,[S]为底物浓度,KM为米氏常数
⑵v是在不同[S]时的反应速度
⑶当底物浓度很低时,V=Vmax*[S]/KM,反应速度与
底物成正比;反之,v≌Vmax,反应速度达最大;再增加
底物浓度,反应速度不受影响。
⒊KM概念:
反应速度达到最大反应速度一半时的作用物浓度。
述:
KM是酶的特征性常数,表示酶与作用物的亲和力大小。
KM越大,酶与作用物的亲和力越小。
同工酶的KM不同。
⒋米氏方程应用
⑴酶的鉴定——根据KM相同与否判定是否同一个酶
⑵酶的纯化——根据KM稳定与否判定酶是否被纯化
⑶计算欲使反应速度达到某一特定反应速度时的合理[S]
(二)Km的意义
⒈KM值等于酶促反应速度达到Vmax一半时的作用物浓度
⒉KM值可反映酶对底物的亲和力,两者呈反比
⒊KM值是酶的特征性常数之一,只与酶的结构、底物和反
应环境(如温度、pH、离子强度)有关,与酶浓度无关。
二、酶浓度对反应速度的影响(课本P33图3-6)
述:
在酶促反应系统中,当[S]足够大时,v∝[E]。
三、温度对反应速度的影响
⒈两者联系:
温度对酶促反应的具有双重影响。
升高温度可加快酶促反应速度,同时也增加酶变性的机会。
述:
温度升高到60℃以上时,大多数酶开始变性;80℃时,多数酶的变性已不可逆。
⒉最适温度
⑴概念:
酶催化活性最大时的环境温度
述:
人体组织中酶的最适温度一般在37-40℃
⑵影响因素:
反应时间
⑶相互关系
①酶可以在较短的时间内耐受较高的温度;
相反,延长反应时间,最适温度变降低。
②环境温度高于最适温度时,反应速度则因酶的变性而降低。
③低温能降低酶活性,但一般不破坏酶;
温度回升后,酶又可以恢复活性。
⒊临床应用:
低温麻醉;低温保存菌种;酶制剂的保存
四、pH对反应速度的影响
⒈原因:
在不同的pH值条件下,酶分子的许多极性基团呈不同的解离状态,而酶活性中心的必需基团往往仅在某一解离状态时才最易同底物结合或具有最大的催化作用。
所以,pH值的改变对酶的催化作用影响很大。
⒉最适pH
⑴概念:
酶催化活性最大时的环境pH
述:
胃蛋白酶的最适pH1.5,精氨酸酶则为9.0。
⑵影响因素:
底物浓度、缓冲液的种类与浓度、酶的纯度等
⑶相互关系
①溶液的pH值高于或低于最适pH时,酶活性降低;
②远离最适pH时,会导致酶的变性失活。
述:
在测定酶的活性时,应选用适宜的缓冲液以保持酶活性
的相对恒定。
五、抑制剂(I)对反应速度的影响
Ⅰ概念:
凡能降低酶的活性而本身不引起酶蛋白变性的物质
Ⅱ种类:
见下表
(一) 不可逆性抑制
⒈概念:
其抑制剂通常与酶活性中心上的必需基团以共价键相结合而使酶失活的抑制作用。
⒉此抑制剂不可用透析法去除
⒊举例:
有机磷农药中毒如605、敌百虫、DDV等。
述:
这类抑制剂与酶活性中心的内、外的必需基团形成牢
固不可逆的共价结合。
重金属和砷制剂与巯基酶结合,故可用BAL(二巯基丙醇)急救。
(二)可逆性抑制
Ⅰ概念:
其抑制剂通过非共价键与酶和(或)酶-底物复合物可逆性结合而使酶活性降低或消失的抑制作用。
Ⅱ抑制剂去除方法:
透析法或超滤法
Ⅲ种类
⒈竞争性抑制
⑴概念:
有些抑制剂与酶的底物结构相似,可与底物竞争酶活性中心,从而阻碍酶与底物结合成中间产物的抑制作用。
⑵特点:
①I与S结构相似,与S竞争结合E的同一部位。
②抑制程度取决于[I]/[S]值及I与E的的亲和力。
⑶动力学特点:
Vmax不变,Km增加
⑷举例:
丙二酸(P35)
⑸应用:
用以阐明某些药物的作用机制(P35)如磺胺类药物
⒉非竞争性抑制
⑴概念:
底物与抑制剂之间无竞争关系,但酶-底物-抑制剂复合物不能进一步释放出产物的抑制作用。
⑵特点:
①I与S结构不相似,结合酶部位与S不同,与酶活性中心外必需基团结合,引起酶构象改变。
②抑制程度只与[I]有关。
⑶动力学特点:
Vmax减小,Km不变
⑷举例:
哇巴因
六、激活剂对酶反应速度的影响
⒈概念:
使酶从无活性变为有活性的或使酶活性增加的物质
述:
如金属离子、氯离子等,它们都能使酶活性增强。
⒉种类
⑴必需激活剂
①概念:
对酶促反应不可缺少的大多数金属离子激活剂
②举例:
Mg2+
⑵非必需激活剂
①概念:
不存在时,酶仍有一定催化活性的某些激活剂
②举例:
Cl-
课外作业:
一、名解:
酶的最适温度;酶的最适pH;不可逆性抑制;可逆性抑制;
竞争性抑制
二、简答:
⒈分别简述酶浓度和底物浓度对酶促反应速度是如何影响的?
⒉什么是米-曼式方程式?
什么是米氏常数?
米氏常数的意义是什么?
⒊何谓酶的竞争性抑制和非竞争性抑制?
试用竞争性抑制的
作用原理阐明磺胺类药物能抑制细菌生长的机理。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 催化 反应 动力学
 冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 负债.pptx
负债.pptx
 关于班级管理建议书.docx
关于班级管理建议书.docx
