 天津市滨海新区学年新高考高一化学下学期期末达标检测试题.docx
天津市滨海新区学年新高考高一化学下学期期末达标检测试题.docx
- 文档编号:10553152
- 上传时间:2023-05-26
- 格式:DOCX
- 页数:50
- 大小:450.21KB
天津市滨海新区学年新高考高一化学下学期期末达标检测试题.docx
《天津市滨海新区学年新高考高一化学下学期期末达标检测试题.docx》由会员分享,可在线阅读,更多相关《天津市滨海新区学年新高考高一化学下学期期末达标检测试题.docx(50页珍藏版)》请在冰点文库上搜索。
天津市滨海新区学年新高考高一化学下学期期末达标检测试题
高一(下)学期期末化学模拟试卷
一、单选题(本题包括20个小题,每小题3分,共60分.每小题只有一个选项符合题意)
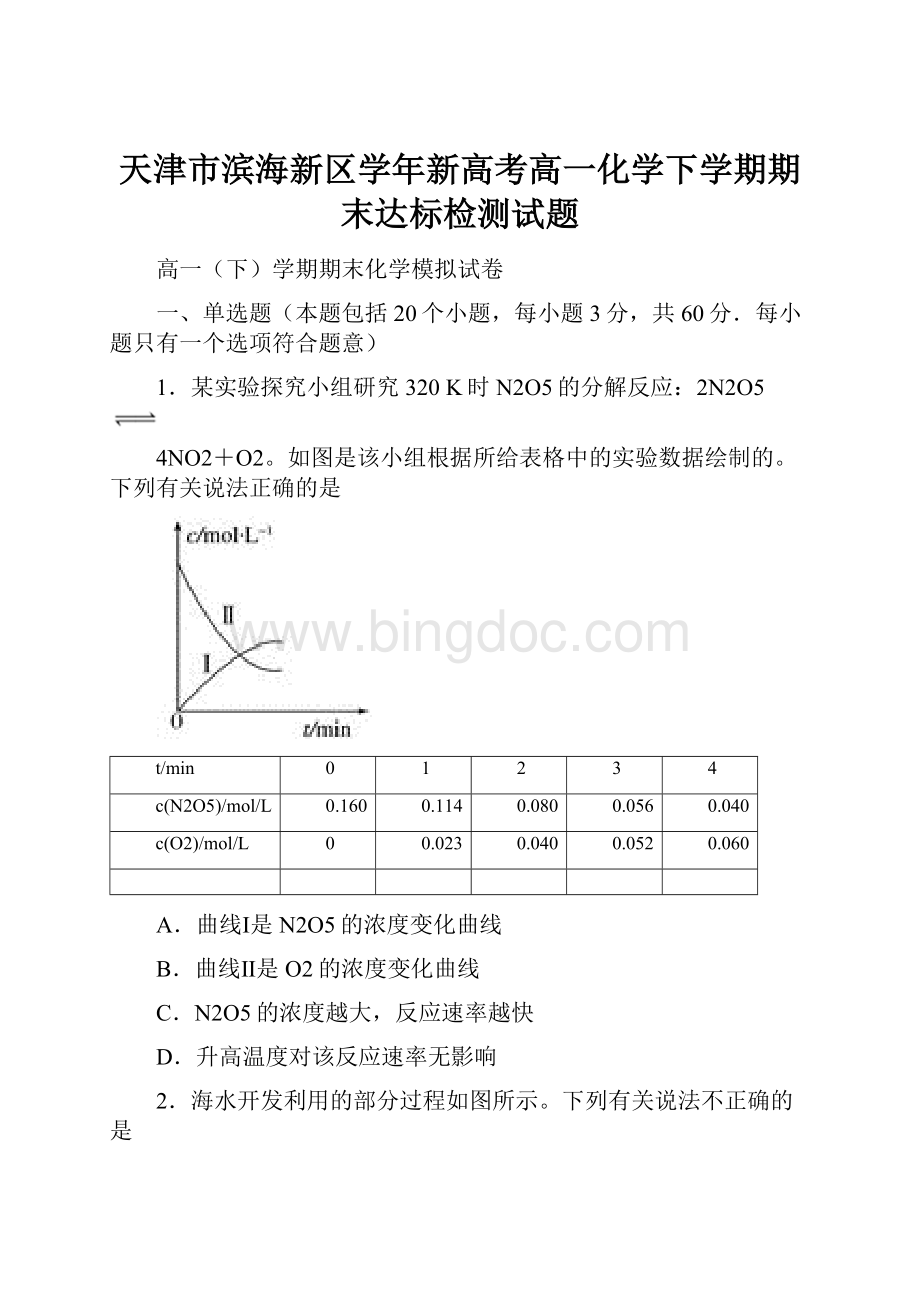
1.某实验探究小组研究320K时N2O5的分解反应:
2N2O5
4NO2+O2。
如图是该小组根据所给表格中的实验数据绘制的。
下列有关说法正确的是
t/min
0
1
2
3
4
c(N2O5)/mol/L
0.160
0.114
0.080
0.056
0.040
c(O2)/mol/L
0
0.023
0.040
0.052
0.060
A.曲线Ⅰ是N2O5的浓度变化曲线
B.曲线Ⅱ是O2的浓度变化曲线
C.N2O5的浓度越大,反应速率越快
D.升高温度对该反应速率无影响
2.海水开发利用的部分过程如图所示。
下列有关说法不正确的是
A.海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等
B.将氯气通入苦卤中发生反应的离子方程式为Cl2+2Br-===2Cl-+Br2
C.在工业上一般选用氢氧化钠溶液作为图示中的沉淀剂
D.某同学设计了如下装置制取无水MgCl2,装置A的作用是制取干燥的HCl气体
3.未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生。
下列属于未来新能源的是()
①天然气②太阳能③风能④石油⑤煤⑥生物质能⑦氢能
A.②③⑥⑦B.①②③④C.①②⑤⑥⑦D.③④⑤⑥⑦
4.将NH3通过灼热的CuO,发现生成一种红色的单质和一种气体单质,这种气体单质是
A.O2B.H2C.N2D.NO
5.日本福岛核电站泄漏的核燃料衰变产物有放射性元素
等,其中
可以用来治疗甲状腺癌,但是如果没有癌症,它也可能诱发甲状腺癌。
下列有关说法中不正确的是()
A.
的原子核所含中子数是78
B.核能的利用证实了原子的可分性
C.
原子和放射性碘原子
互为同位素
D.
原子和碘
原子的质子数不同
6.下列物质中,不属于通常所说的三大合成材料的是
A.塑料B.蛋白质C.合成纤维D.合成橡胶
7.关于1mol/LK2SO4溶液的下列说法正确的是()
A.溶液中含有1molK2SO4B.可由1molK2SO4溶于1L水得到
C.溶液中c(K+)=2mol/LD.1L溶液中含2molK+,2molSO42-
8.已知反应A+B
C+D的能量变化如图所示,下列说法正确的是
A.产物C的能量高于反应物的总能量
B.若该反应中有电子得失,则可设计成原电池
C.反应物的总能量低于生成物的总能量
D.该反应中的反应物A和B的转化率定相同
9.下列叙述正确的是( )
A.分子式相同,各元素质量分数也相同的物质是同种物质
B.通式相同的不同物质一定属于同系物
C.分子式相同的不同物质一定是同分异构体
D.相对分子质量相同的不同物质一定是同分异构体
10.下列说法正确的是()
A.
结论:
CH4的燃烧热为1.3kJ/mol
B.
(灰锡为粉末状)结论:
锡制品在寒冷的冬天因易转化为灰锡而损坏
C.稀溶液中有
结论:
将盐酸与氨水的稀溶液混合后,若生成1molH20,则会放出2.3kJ的能量
D.
AH=一3.5kJ/mol,
结论:
相同条件下金刚石性质比石墨稳定
11.下列化学用语的使用正确的是:
A.N2的结构式:
N-NB.CO2的比例模型:
C.氯化氢的电子式:
D.乙烯的球棍模型:
12.下列关于化学能与其它能量相互转化的说法不正确的是( )
A.化学反应过程中既发生物质变化,也发生能量变化
B.可逆反应的正反应若是放热反应,则其逆反应必然是吸热反应
C.图
所示装置不能将化学能转化为电能
D.图
所示的反应无需加热都能发生
13.某地有甲.乙两工厂排放污水,污水中各含有下列8种离子中的4种(两厂不含相同离子):
Ag+.Ba2+.Fe3+.Na+.Cl-.CO32-.NO3-.OH-。
若两厂单独排放都会造成严重的水污染,如将两厂的污水按一定比例混合,沉淀后污水便变成无色澄清只含硝酸钠而排放,污染程度会大大降低。
关于污染源的分析,你认为正确的是
A.CO32-和NO3-可能来自同一工厂B.Na+和NO3-来自同一工厂
C.Ag+和Na+可能来自同一工厂D.Cl-和NO3-一定不在同一工厂
14.北京奥运会开幕式在李宁点燃鸟巢主火炬时达到高潮。
奥运火炬采用的是环保型燃料—丙烷,其燃烧时发生反应的化学方程式为C3H8+5O2
3CO2+4H2O。
下列说法中不正确的是( )
A.火炬燃烧时化学能只转化为热能
B.所有的燃烧反应都会释放热量
C.1molC3H8和5molO2所具有的总能量大于3molCO2和4molH2O所具有的总能量
D.丙烷完全燃烧的产物对环境无污染,故丙烷为环保型燃料
15.下列各图所示的分子结构模型中,分子式为CH4的是( )
A.
B.
C.
D.
16.为纪念DmitriMendeleev发明的元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。
a、b、c、d、四种短周期元素分别位于三个周期,其原子的最外层电子数和原子半径之间的关系如图所示。
下列说法中错误的是
A.a为氢元素
B.原子半径c C.b的最高价氧化物对应的水化物为强酸 D.a与c组成的一种化合物中既含极性键又含非极性键 17.下列有关反应速率的说法正确的是( ) A.用铁片和稀硫酸反应制氢气时,改用98%的浓硫酸可以加快反应速率 B.其他条件不变时,增大压强,活化分子百分数增大,化学反应速率加快 C.在碳酸钙和盐酸反应中,加多些碳酸钙可使反应速率明显加快 D.一定量的稀盐酸跟过量锌粉反应时,为了加快反应速率又不影响生成H2的总量,可采取加入少量CuSO4溶液 18.NA表示阿伏加德罗常数的值,下列说法正确的是 A.5.6g铁粉在足量盐酸中完全溶解,转移电子数为0.3NA B.0.2mol浓硫酸与足量铜反应,转移电子数为0.2NA C.7.8gNa2O2与足量二氧化碳反应转移电子数为0.1NA D.NA个HF分于在标准状况下的体积为22.4L 19.(6分)下列有关化学用语,使用正确的是 A.氯原子的原子结构示意图: B.NH4Cl的电子式: C.原子核内有10个中子的氧原子: D.聚乙烯的结构简式: CH2=CH2 20.(6分)X元素的阳离子和Y元素的阴离子具有与氖原子相同的电子层结构,下列说法正确的是 A.原子序数: X B.原子半径: X>Y C.原子的最外层电子数: X>Y D.得电子能力: X>Y 二、计算题(本题包括1个小题,共10分) 21.(6分)镁及其合金是一种用途广泛的金属材料,目前世界上60%的镁是从海水中提取的。 主要步骤如下: (1)镁在元素周期表中位于第__________周期,第___________族。 (2)为使MgSO4完全转化为Mg(OH)2沉淀,试剂①可选用____________(填化学式),且加入试剂①的量应______________(选填“少量”或“过量”)。 (3)若要检验溶液A中含有的SO42-,使用的试剂是_________________。 (4)加入试剂①后,分离得到Mg(OH)2沉淀的方法是__________。 试剂②可以选用_______。 (5)反应①、反应②、反应③属于氧化还原反应类型的是________。 (6)工业上常用电解熔融MgCl2的方法冶炼得到金属Mg,写出该反应的化学方程式__________。 三、实验题(本题包括1个小题,共10分) 22.(8分)实验室可以用下图所示的装置制取乙酸乙酯。 回答下列问题: (1)在试管中配制一定比例的乙醇、乙酸和浓硫酸的混合溶液,其方法是: _______; (2)乙酸乙酯在饱和碳酸钠溶液的_______层;(填“上”或“下”) (3)浓硫酸的作用是______________; (4)制取乙酸乙酯的化学方程式是______,该反应属于___(填反应类型)反应; (5)饱和碳酸钠的作用是: ________________; (6)生成乙酸乙酯的反应是可逆反应,反应一段时间后,就达到了该反应的限度。 下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号)_________。 ①混合物中各物质的浓度不再变化; ②单位时间里,生成1mol乙醇,同时生成1mol乙酸; ③单位时间里,生成1mol乙酸乙酯,同时生成1mol乙醇。 四、推断题(本题包括1个小题,共10分) 23.(8分)下表中列出五种短周期元素A、B、C、D、E的信息,请推断后回答: 元素 有关信息 A 元素主要化合价为-2,原子半径为0.074nm B 所在主族序数与所在周期序数之差为4,形成的单质是黄绿色有毒气体 C 原子半径为 ,其单质为黄色固体,可在A的单质中燃烧 D 最高价氧化物的水化物能按 电离出电子数相等的阴、阳离子 E 原子半径为 ,最高价氧化物的水化物可与其氢化物形成一种盐X (1)写出C元素在周期表中的位置_________________,写出D元素最高价氧化物的水化物电子式________________。 (2)写出A与C元素气态氢化物的稳定性由大到小的顺序是______________ 填化学式 。 (3)写出B与C元素最高价氧化物的水化物酸性由弱到强的顺序是_________ 填化学式 。 (4)写出D的单质在氧气中燃烧生成产物为淡黄色固体,该氧化物含有的化学键类型是________________。 (5)砷 与E同一主族,As原子比E原子多两个电子层,则As的原子序数为_______,其氢化物的化学式为___________。 五、综合题(本题包括1个小题,共10分) 24.(10分)化学反应速率和限度与生产、生活密切相关. (1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水法收集反应放出的氢气,实验记录如下(累计值): 时间 1 2 3 4 5 氢气体积/mL(标况) 100 240 464 576 620 ①哪一段时间内反应速率最大: ____min(填“0~1”“1~2”“2~3”“3~4”或“4~5”)。 ②3~4min内以盐酸的浓度变化来表示的该反应速率______(设溶液体积不变)。 (2)另一学生为控制反应速率防止反应过快难以测量氢气体积.他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量.你认为不可行的是____(填字母)。 A蒸馏水BKCl洛液C浓盐酸DCuSO4溶液 (3)在4L密闭容器中,X、Y、Z三种气体的物质的量随时间变化曲线如图。 ①该反应的化学方程式是_______________。 ②该反应达到平衡状态的标志是___________(填字母)。 AY的体积分数在混合气体中保持不变BX,、Y的反应速率比为3: 1 C容器内气体压强保持不变D容器内气体的总质量保持不变 E生成1molY的同时消耗2molZ ③2min内Y的转化率为__________。 参考答案 一、单选题(本题包括20个小题,每小题3分,共60分.每小题只有一个选项符合题意) 1.C 【解析】 【分析】 结合题给的曲线和表格中0min时的数据,可以判断该反应是从反应物开始投料的,直至建立平衡状态。 N2O5的速率从最大逐渐减小至不变,O2的速率从最小逐渐增大至最大而后不变。 【详解】 A.曲线Ⅰ是O2的浓度变化曲线,A项错误; B.曲线Ⅱ是N2O5的浓度变化曲线,B项错误; C.因从反应物开始投料,所以随N2O5的浓度减小,化学反应速率逐渐减小,直至平衡时化学反应速率保持不变,所以N2O5的浓度越大,反应速率越快,C项正确; D.升高温度,反应速率加快,D项错误; 所以答案选择C项。 2.C 【解析】分析: A.蒸馏法、电渗析法、离子交换法都可用于淡化海水,据此分析判断;B.根据苦卤中主要含有溴的化合物分析判断;C.根据氢氧化钠和氢氧化钙的工业成本分析判断;D.根据氯化镁加热时能够水解分析判断。 详解: A.蒸馏法是把水从水的混合物中分离出来,得到纯净的水,通过离子交换树脂可以除去海水中的离子,从而达到淡化海水的目的,利用电渗析法可使相应的离子通过半透膜以达到硬水软化的效果,故A正确;B.苦卤中主要含有溴的化合物,将氯气通入苦卤中发生反应的离子方程式为Cl2+2Br-===2Cl-+Br2,故B正确;C.在工业上一般选用氢氧化钙作为沉淀剂,氢氧化钙可以通过加热分解石灰石或贝壳得到,成本较低,故C错误;D.氯化镁加热时能够水解,生成的氯化氢易挥发,会促进水解,因此用如图装置制取无水MgCl2,需要在干燥的HCl气体的气氛中进行,故D正确;故选C。 点睛: 本题考查了元素及其化合物的性质和物质的分离与提纯。 本题的易错点为D,要注意盐类水解知识的应用。 3.A 【解析】 【分析】 新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生,据此判断。 【详解】 煤、石油、天然气是化石能源,不是新能源,常见新能源有: 太阳能、核能、地热能、潮汐能、风能、氢能、生物质能等。 答案选A。 4.C 【解析】 【详解】 将NH3通过灼热的CuO,发现生成一种红色的单质和一种气体单质,红色的单质为铜,铜元素的化合价降低,根据氧化还原反应的规律和质量守恒,N元素的化合价升高,气体单质只能为氮气,故选C。 5.D 【解析】本题考查同位素。 详解: 的原子核质量数为131,质子数为53,所含中子数是(131—53)=78,A正确;核能的利用证实原子的可分性,B正确;127I和131I的质子数相同,中子数不同,所以127I和131I是同位素,C正确; 原子和碘 原子的质子数都为53,D错误。 故选D。 点睛: 对于原子来说: 核内质子数=核外电子数=核电荷数,相对原子质量=核内质子数+核内中子数,要熟记这两个等式。 6.B 【解析】试题分析: 通常所说的三大合成材料的是合成纤维、合成橡胶和合成塑料,蛋白质不是通常所说的三大合成材料,答案选B。 考点: 考查常识性知识的考查,难度不大。 试题属于识记性知识的考查,记住即可。 点评: 7.C 【解析】 【详解】 A.没有告诉溶液体积,无法计算K2SO4的物质的量,故A错误; B.1molK2SO4溶于1L水中,溶液体积不是1L,溶液浓度不是1mol/L,故B错误; C.溶液中c(K+)=2c(K2SO4)=2mol•L-1,故C正确; D.1L1mol•L-1K2SO4溶液中含有1molK2SO4,含有2molK+、1molSO42-,故D错误; 故答案选C。 【点睛】 本题考查物质的量浓度的计算,明确物质的量浓度的概念及表达式即可解答,选项A、B为解答的易错点,试题侧重基础知识的考查。 8.C 【解析】 【详解】 A.图象分析可以知道,反应物能量低于生成物,反应为吸热反应,反应物总能量+吸收的热量=生成物总能量,产物C的能量不一定高于反应物的总能量,A错误; B.若该反应中有电子得失为氧化还原反应,但是反应是吸热反应,不能自发进行,非自发进行的氧化还原反应不能设计为原电池,B错误; C.当反应物的总能量低于生成物的总能量时,反应的的焓变为正值,反应为吸热反应,符合图象变化,C正确; D.反应物A和B的转化率和起始量变化量有关,若起始量不同,转化率也不同,D错误; 正确选项C。 9.C 【解析】 【详解】 A、也可能是同分异构体,不正确; B、结构相似,分子组成相差若干个CH2原子团的物质,互称为同系物,因此同系物的通式相同,但通式相同的不一定是同系物,B不正确。 C、分子式相同,而结构不同的化合物是同分异构体,C正确。 D、相对分子质量相同,但分子式不一定相同,不正确。 答案选C。 10.B 【解析】分析: A、根据燃烧热的概念来回答;B、降温平衡逆向移动;C、强酸和强碱反应生成1mol水放出的热量为中和热.D、石墨比金刚石能量低,稳定。 详解: A、燃烧热是生成稳定的产物(液态水)放出的热量,不能是气态水,故A错误;B、降温平衡逆向移动,锡制品在寒冷的冬天因易转化为灰锡而损坏,故B正确;C、一水合氨是弱碱,故C错误;D、两式相减得C(石墨,s)═C(金刚石,s)△H>0,石墨能量小于金刚石,则金刚石比石墨活泼,石墨比金刚石稳定,故D错误;故选B 点睛: 本题考查了热化学方程式的书写方法,燃烧热,中和热概念分析应用,解题关键: 掌握概念实质,易错点C,强酸和强碱反应生成1mol水放出的热量为中和热,一水合氨是弱碱。 难点D,物质所具有的能量越低越稳定。 11.D 【解析】 【详解】 A.N2的结构式为N≡N,A错误; B.碳原子半径大于氧原子半径,则 不能表示CO2的比例模型,B错误; C.氯化氢是共价化合物,电子式为 ,C错误; D.乙烯的球棍模型为 ,D正确; 答案选D。 【点睛】 选项B是易错点,学生往往只从表面看满足CO2是直线形结构,但忽略了碳原子半径和氧原子半径的大小关系。 12.D 【解析】 【详解】 A.化学反应过程中既发生物质变化,也发生能量变化,A正确; B.可逆反应的正反应若是放热反应,则其逆反应必然是吸热反应,B正确; C.图 所示装置没有盐桥,无法构成闭合回路,不能将化学能转化为电能,C正确; D.图 所示的反应为放热反应,但并不是所有的放热反应都无需加热,如燃烧反应等,D错误; 故答案选D。 【点睛】 反应是吸热还是放热,与反应条件无关。 13.D 【解析】 【分析】 假设甲厂排放的污水中含有Ag+,根据离子共存,甲厂一定不含CO32-、OH-、Cl-则CO32-、OH-、Cl-应存在与乙厂;因Ba2+与CO32-、Fe3+与OH-不能共存,则Fe3+、Ba2+存在于甲厂,根据溶液呈电中性可以知道,甲厂一定存在阴离子NO3-;所以甲厂含有的离子有: Ag+、Fe3+、Ba2+、NO3-,乙厂含有的离子为: Na+、CO32-、OH-、Cl-,据此分析解答。 【详解】 A.根据以上分析可以知道,CO32-离子和NO3-不可能来自同一工厂,故A错误; B.由分析可以知道,Na+和NO3-一定来自不同的工厂,故B错误; C.Ag+和Na+一定来自不同工厂,故C错误; D.根据分析可以知道,Cl-和NO3-一定来自不同工厂,所以D选项是正确的。 答案选D。 14.A 【解析】 【详解】 A、火炬燃烧时,不仅发热,而且发光.所以火炬燃烧时,化学能不仅转化为热能,还转化为光能等其它形式的能,A项错误; B、所有的燃烧反应都是放热反应,都会释放热量,B项正确; C、根据能量守恒定律,如果反应物所具有的总能量高于生成物所具有的总能量,在反应中有一部分能量转变为热能的形式释放,这就是放热反应。 所有的燃烧反应都是放热反应,丙烷的燃烧是放热反应,所以1molC3H8和5molO2所具有的总能量大于3molCO2和4molH2O所具有的总能量,C项正确; D、丙烷完全燃烧C3H8+5O2 3CO2+4H2O的产物二氧化碳和水,对环境无污染,故丙烷为环保型燃料,故D正确。 答案选A。 15.A 【解析】 【详解】 A、根据分子的结构模型可知,该有机物为甲烷,分子式为CH4,故A正确; B、根据分子的结构模型可知,该有机物为乙烯,分子式为C2H4,故B错误; C、根据分子的结构模型可知,该有机物为乙醇,分子式为C2H6O,故C错误; D、根据分子的结构模型可知,该有机物为苯,分子式为C6H6,故D错误; 答案选A。 16.C 【解析】 【分析】 题中已经说明四种短周期元素分别为三个周期。 同一周期中,从左到右,随着原子序数的增大,原子最外层的电子数也要增大,原子半径在逐渐减小。 a的化合价为1,且原子半径是最小的,则a一定是H;d的原子半径比c大,最外层电子数比c多,则c一定在第二周期,d在第三周期;c、d的最外层电子数分别为4和6,则c为C,d为S;b的原子半径最大,最外层电子数为1,则b为Na。 综上所述,a为H,b为Na,c为C,d为S。 【详解】 A.a为H,b为Na,c为C,d为S,A正确; B.如图所示,c的原子半径小于d,B正确; C.b的最高价氧化物对应的水化物是NaOH,是强碱,C错误; D.a、c组成的化合物中,除了甲烷之外,都具有C-C键和C-H键,即含极性键和非极性键,D正确; 故合理选项为C。 【点睛】 要注意题中是否说明是短周期元素。 此外,再根据元素周期律推断出各个元素。 17.D 【解析】 【详解】 A、铁与浓硫酸发生钝化反应,改用98%的浓硫酸不能加快反应速率,故A不符合题意; B、其他条件不变,增大压强,增加单位体积内活化分子的个数,使化学反应速率加快,故B不符合题意; C、碳酸钙是固体,浓度视为常数,即多加些碳酸钙不能使反应速率明显加快,故C不符合题意; D、加入少量的CuSO4,发生Zn+CuSO4=ZnSO4+Cu,构成原电池,加快反应速率,锌粉是过量,即也不影响生成H2的总量,故D符合题意; 答案选D。 18.C 【解析】A.5.6g铁粉是0.1mol,在足量盐酸中完全溶解生成氯化亚铁和氢气,转移电子数为0.2NA,A错误;B.0.2mol浓硫酸与足量铜反应,由于随着反应的进行,硫酸浓度减小,稀硫酸与铜不反应,因此转移电子数小于0.2NA,B错误;C.7.8gNa2O2是0.1mol,与足量二氧化碳反应转移电子数为0.1NA,C正确;D.NA个HF分于是1mol,在标准状况下HF不是气体,其体积不是22.4L,D错误,答案选C。 点睛: 要准确把握阿伏加德罗常数的应用,一要认真理清知识的联系,关注状况条件和物质状态、准确运用物质结构计算、电离和水解知识的融入、留心特殊的化学反应,如本题中Na2O2与CO2的反应、阿伏加德罗定律和化学平衡的应用。 避免粗枝大叶不求甚解,做题时才能有的放矢。 二要学会留心关键字词,做题时谨慎细致,避免急于求成而忽略问题的本质。 必须以阿伏加德罗常数为基础点进行辐射,将相关知识总结归纳,在准确把握各量与阿伏加德罗常数之间关系的前提下,着重关注易错点,并通过练习加强理解掌握,这样才能通过复习切实提高得分率。 19.C 【解析】 A.氯原子的核外电子数是17,原子结构示意图: ,A错误;B.NH4C1是离子化合物,电子式: ,B错误;C.原子核内有10个中子的氧原子可表示为 ,C正确;D.乙烯的结构式: ,D错误。 答案选C。 点睛: 注意了解有机物结构的常见表示方法, (1)结构式: 完整的表示出有机物分子中每个原子的成键情况。 (2)结构简式: 结构式的缩简形式。 结构式中表示单键的“—”可以省略,“C=C”和“C≡C”不能省略。 醛基、羧基则可简写为—CHO和—COOH。 (3)键线式: 写键线式要注意的几个问题: ①一般表示3个以上碳原子的有机物;②只忽略C—H键,其余的化学键不能忽略;③必须表示出C=C、C≡C键等官能团;④碳氢原子不标注,其余原子必须标注(含羟基、醛基和羧基中氢原子);⑤计算分子式时不能忘记顶端的碳原子。 另外还需要注意球
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 天津市 滨海新区 学年 新高 高一化学 学期 期末 达标 检测 试题
 冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《大侦探小卡莱》读后感.docx
《大侦探小卡莱》读后感.docx
