 灵芝孢子油软胶囊生产工艺和质量标准.docx
灵芝孢子油软胶囊生产工艺和质量标准.docx
- 文档编号:2958463
- 上传时间:2023-05-05
- 格式:DOCX
- 页数:13
- 大小:70.43KB
灵芝孢子油软胶囊生产工艺和质量标准.docx
《灵芝孢子油软胶囊生产工艺和质量标准.docx》由会员分享,可在线阅读,更多相关《灵芝孢子油软胶囊生产工艺和质量标准.docx(13页珍藏版)》请在冰点文库上搜索。
灵芝孢子油软胶囊生产工艺和质量标准
《灵芝孢子油软胶囊生产工艺和质量标准》
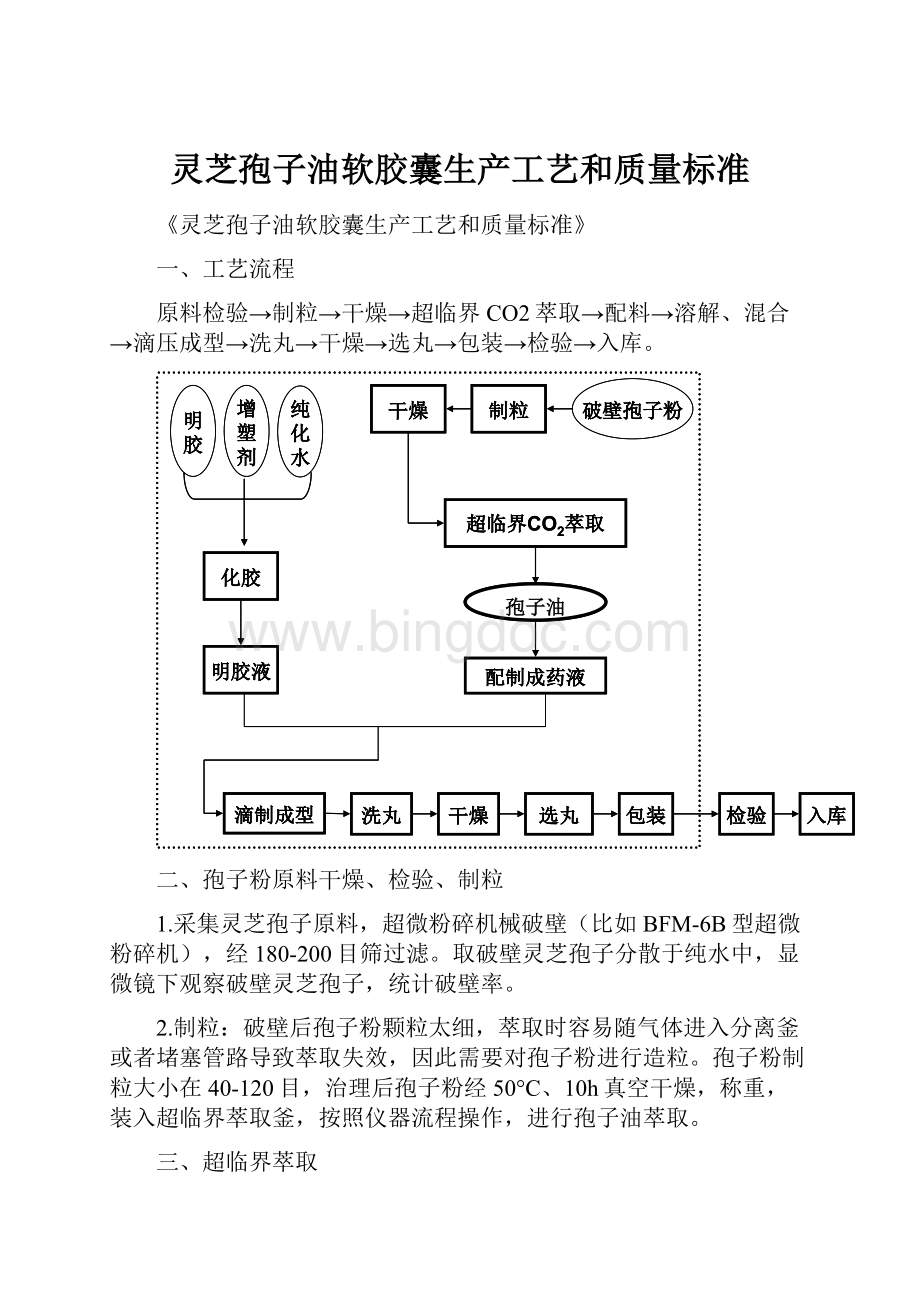
一、工艺流程
原料检验→制粒→干燥→超临界CO2萃取→配料→溶解、混合→滴压成型→洗丸→干燥→选丸→包装→检验→入库。
二、孢子粉原料干燥、检验、制粒
1.采集灵芝孢子原料,超微粉碎机械破壁(比如BFM-6B型超微粉碎机),经180-200目筛过滤。
取破壁灵芝孢子分散于纯水中,显微镜下观察破壁灵芝孢子,统计破壁率。
2.制粒:
破壁后孢子粉颗粒太细,萃取时容易随气体进入分离釜或者堵塞管路导致萃取失效,因此需要对孢子粉进行造粒。
孢子粉制粒大小在40-120目,治理后孢子粉经50°C、10h真空干燥,称重,装入超临界萃取釜,按照仪器流程操作,进行孢子油萃取。
三、超临界萃取
CO2超临界萃取装置,优选出超临界萃取条件,例如温度、压力、时间以及添加剂用量等。
参考的最佳萃取条件:
压力28MPa,温度45°C,气体流量为35kg/h,添加剂17%。
灵芝孢子油萃取:
1.将破壁的灵芝孢子粉放入萃取釜中;
2.利用制冷系统制备零下5度的液态二氧化碳储存于液罐中,压力达到4-5MPa;
3.调节频率在25HZ-30HZ(流量控制),萃取釜温度在45度,压力25MPa,用高压泵将液态
二氧化碳通过萃取釜进行萃取;
4.调节分离室1的温度在40度,压力8MPa,分离室2的温度在40度,压力5MPa,收集萃取
出的孢子油;
5.萃取过程2-4小时(当出油速度低于5ml/小时时停止)。
四、配制成药液
填充物本身是油类的,只需加入适量抑菌剂,或再添加一定数量的玉米油(或PEG400),混匀即得。
五、软胶囊的制法
软胶囊囊材是用明胶、甘油、增塑剂、防腐剂、遮光剂、色素和其它适宜的药用材料制成。
1.化胶
软胶囊壳主要含明胶、阿拉伯胶、增塑剂、防腐剂(如山梨酸钾、尼泊金等)、遮光剂和色素等成分,其中明胶:
甘油:
水为1:
0.3~0.4:
0.7~1.4的比例为宜,根据生产需要,按上述比例,将以上物料加入夹层罐中搅拌,蒸汽夹层加热,使其溶化,保温1~2小时,静置待泡沫上浮后,保温过滤,成为胶浆备用。
2.滴制成型
采用滴制机生产软胶囊剂,将油料加入料斗中;明胶浆加入胶浆斗中,并保持一定温度;盛软胶囊器中放入冷却液(必须安全无害,和明胶不相混溶,一般为液体石蜡、植物油、硅油等),根据每一胶丸内含药量多少,调节好出料口和出胶口,胶浆、油料先后以不同的速度从同心管出口滴出,明胶在外层,药液从中心管滴出,明胶浆先滴到液体石蜡上面并展开,油料立即滴在刚刚展开的明胶表面上,由于重力加速度的道理,胶皮继续下降,使胶皮完全封口,油料便被包裹在胶皮里面,再加上表面张力作用,使胶皮成为圆球形,由于温度不断的下降,逐渐凝固成软胶囊,将制得的胶丸在室温(20~30度)冷风干燥,再经石油醚洗涤两次,再经过95%乙醇洗涤后于30~35度烘干,直至水分合格后为止,即得软胶囊。
制备过程中必须控制药液、明胶和冷却液三者的密度以保证胶囊的有一定的沉降速度,同时有足够的时间冷却。
浙江新昌制药生产全套软胶囊设备,包括双滴头软胶囊机、滚筒干燥机、冷冻机、烊胶桶、揩丸机等全套设备。
六、软胶囊干燥、清洗工艺
1.软胶囊干燥定型转笼
软胶囊干燥定型转笼是用于对主机压制的合格胶丸经输送机送入干燥转笼内进行干燥定形。
干燥机可一节也可多节串联组成,能顺时转与逆向转动。
干燥箱一端由鼓风机输出恒温的空调风以保证软胶丸干燥之用。
2.XWJ-II型超声波软胶囊清洗机
该设备可对软胶囊进行一次性清洗,并且整个过程不会出现挤压现象。
清洗过程分为:
超声波浸洗、浸泡、丸体与酒精分离、喷淋四个步骤。
七、生产工艺环境要求
软胶囊工艺室:
温度22-24℃,相对湿度20%
软胶囊干燥室:
温度22-24℃,相对湿度20%
软胶囊检测室:
温度22-24℃,相对湿度35%
灵芝孢子油软胶囊
1 范围
本标准规定了灵芝孢子油软胶囊的技术要求、食品添加剂、生产加工过程卫生要求、检验方法、检验规则、标志、标签、包装、运输及贮存。
本标准适用于以灵芝孢子粉提取物(孢子油)、明胶、纯化水为主要原料,经溶解、混合、压丸、洗丸、干燥、选丸、包装等生产加工工艺精制而成的灵芝孢子油软胶囊。
本标准适用于灵芝孢子油软胶囊的生产、检验和销售。
2 规范性引用文件
下列文件中引用的条款对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅所注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T191
包装储运图示标志
GB2760
食品安全国家标准食品添加剂使用标准
GB4789.2
食品微生物学检验菌落总数测定
GB4789.3
食品微生物学检验大肠菌群计数
GB4789.4
食品微生物学检验沙门氏菌检验
GB/T4789.5
食品卫生微生物学检验志贺氏菌检验
GB4789.10
食品微生物学检验金黄色葡萄球菌检验
GB/T4789.11
食品微生物学检验溶血性链球菌检验
GB4789.15
食品微生物学检验霉菌和酵母计数
GB5009.3
食品中水分的测定
GB5009.5
食品中蛋白质的测定
GB/T5009.11
食品中总砷及无机砷的测定
GB5009.12
食品中铅的测定
GB/T5009.37
食用植物油卫生标准的分析方法
GB/T5009.123
食品中铬的测定
GB/T5530
动植物油脂酸值和酸度测定
GB/T6543
运输包装用单瓦楞纸箱和双瓦楞纸箱
GB/T6783
食品添加剂明胶
GB7718
预包装食品标签通则
GB9687
食品包装用聚乙烯成型品卫生标准
GB10621
食品添加剂液体二氧化碳
GB14881
食品企业通用卫生规范
JJF1070
定量包装商品净含量计量检验规则
3 技术要求
3.1 原料及辅料
孢子粉
应符合附录A的要求
明胶
应符合GB/T6783规定的相关要求。
食品级液体二氧化碳
应符合GB10621规定的相关要求。
3.2 生产工艺
原料检验→制粒→干燥→超临界CO2萃取→配料→溶解、混合→压丸→洗丸→干燥→选丸→包装→检验→入库。
3.3 感官指标
感官指标应符合表1的规定
表1感官指标
项目
指标
色泽
棕褐色胶囊,有光泽,色泽均匀一致。
滋味和气味
具有产品特有的滋味和气味,无酸败等异味。
形态
胶囊,内容物为金黄色半透明油状液体,无明显异物。
3.4 特有营养成分指标
特有营养成分指标应符合表2的要求。
表2特有营养成分指标
项目
指标
多糖,%≥
6
三萜类化合物,%≥
15
3.5 理化指标
理化指标应符合表3的规定。
表3理化指标
项目
指标
水分,%≤
5
蛋白质,%≥
4
酸价,mgKOH/g≤
40.0
过氧化值,%≤
0.2
铅(以Pb计),mg/kg≤
1.0
砷(以As计),≤
0.5
铬(以Cr计),mg/kg≤
1.0
3.6 微生物指标
微生物指标应符合表4的要求。
表4微生物学指标
项目
指标
菌落总数,,cfu/g≤
3000
大肠菌群,MPN/100g≤
40
霉菌和酵母,cfu/g≤
30
致病菌(沙门氏菌、志贺氏菌、金黄色葡萄球菌、溶血性链球菌)
不得检出
3.7 净含量及允许短缺量
应符合JJF1070的规定。
4 食品添加剂
4.1 食品添加剂的品种和使用量应符合GB2760的规定。
4.2 食品添加剂质量应符合相应的标准和规定。
5 加工和生产过程的卫生要求
产品加工和生产过程卫生要求应符合GB14881的规定。
6 试验方法
6.1 感官指标检验
取样品20粒,剥开,内容物在自然光下,用肉眼观察其色泽、性状,闻其香气、品尝滋味,其性状及色香味应符合表1的要求。
6.2 特有营养成分指标
多糖
按附录B规定的方法检验测定。
三萜类化合物
按附录C规定的方法检验测定。
6.3 理化检验指标
水分
按GB5009.3检验测定。
蛋白质
按GB5009.5检验测定。
酸价
按GB/T5530检验测定。
过氧化值
参照GB/T5009.37及附录D规定的方法检验测定。
铅
按GB5009.12检验测定。
砷
按GB/T5009.11检验测定。
铬
按GB/T5009.123检验测定。
6.4 微生物指标
菌落总数
按GB4789.2规定的方法测定。
大肠菌群
按GB4789.3规定的方法测定。
霉菌和酵母
按GB4789.15规定的方法测定。
致病菌(沙门氏菌、志贺氏菌、金黄色葡萄球菌、溶血性链球菌)
按GB/T4789.4、GB/T4789.5、GB/T4789.10、GB/T4789.11规定的方法测定。
6.5 净含量
从抽取的样品中至少取10粒胶囊,逐粒称重精确至0.001g,倒出内容物,用乙醚冲洗附着在胶囊壳上的内容物,置通风处使溶剂完全挥发,再精确称取胶囊壳质量,分别计算每粒质量之差即为内容物含量,结果以平均值计算净含量。
7 检验规则
7.1 原料入库检验
原料入库前应由厂技术检验部门按原料要求标准检验,合格后方可入库使用。
7.2 出厂检验
本产品由生产厂的质量监督检验部门按本标准的规定进行检验,合格后方可出厂。
生产厂应保证所有出厂的产品都符合本标准的要求。
每批出厂的产品都应附有种类证明书。
取样方法
以同一次配料,同一班次生产包装好的产品为一批,同一批号产品中,在检验外部包装后,按表5规定挑出一定件数进行取样(或每批抽取样品为产品总数百万分之一,不满一万者亦以万计)。
表5样品抽样方法
每批产品的包装件数
应抽样件数
1-5件
全检
6-50件
5件
51-100件
10件
101-500件
15件
501-1000件
20件
出厂检验项目
出厂检验项目为感官指标、酸价、微生物指标、功效成分等为必检项目。
7.3 型式检验
型式检验项目为技术要求中的全部项目。
型式检验至少每年进行一次,有下列情况之一时应进行型式检验。
A.质量监督检验机构提出进行型式检验要求时。
B.出厂检验结果与上次型式检验有较大差异时。
C.停产半年以上恢复生产时。
D.原料产地变化或改变主要生产工艺,可能影响产品质量时。
7.4 判定规则
出厂检验判定规则
出厂检验项目全部符合标准,判定为合格品;出厂检验结果有一项(微生物除外)不符合本标准要求时,应加倍取样复检,复检结果符合要求时,作合格论,如有一项指标不符合本标准要求时,则整批产品不合格。
微生物有一项不符合本标准,判为不合格品,不应复检。
型式检验判定规则
型式检验项目全部符合本标准,判为合格品。
型式检验项目不超过3项(微生物除外)不符合本标准,可以加倍取样复检,复检结果有一项指标不符合本标准要求时,判为不合格。
微生物项目有一项不符合本标准,判为不合格品,不应复检。
8 标志、标签、包装、运输和贮存
8.1 标志、标签
产品的销售包装标签应符合GB7718的规定。
产品运输包装上应标注:
食品名称、执行标准、净含量、数量规格、生产单位名称、地址、生产日期、并有“防潮”、“防晒”、“防雨淋”等标志,应符合GB/T191的规定。
8.2 包装
内包装采用聚乙烯烯(PE)塑料瓶,内包装瓶应符合GB9687的要求。
本产品的外包装采用瓦楞纸箱,纸箱应符合GB/T6543的要求,外包装上应印有产品名称、生产企业名称、生产日期、保质期,箱内必须有产品合格证或产品质量检验证。
8.3 运输
运输工具应清洁、干燥,在运输过程中产品不应与有毒、有害、有腐蚀性、易挥发或有异味物品混装运输。
运输过程中不得暴晒、雨淋、受潮、冰冻。
8.4 贮存
贮存产品的仓库应保持清洁、阴凉干燥通风,不得暴露堆放、日晒、雨淋。
产品不得与潮湿地面接触,包装箱底部应离地面10cm。
产品不得与有毒、有害、有腐蚀性、易挥发或有异味物品同库贮存。
9 保质期
在本标准规定的条件下,保质期为24个月。
附 录 A
(规范性附录)
附录A原辅料要求
A1.灵芝孢子粉:
符合以下要求
项目
指标
性状
咖啡色粉末,具产品特有香味
破壁率,%≥
80
含油率,%≥
20
多糖含量,%≥
40.0
水分,%≤
5.0
灰分,%≤
5.0
重金属,ppm≤
15
菌落总数,cfu/g≤
1000
大肠菌群,MPN/100g≤
30
霉菌和酵母,cfu/g≤
30
致病菌(沙门氏菌、志贺氏菌、金黄色葡萄球菌)≤
不得检出
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 灵芝 孢子 软胶囊 生产工艺 质量标准
 冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 整编新型生态农业旅游休闲农庄项目发展建设市场研究报告.docx
整编新型生态农业旅游休闲农庄项目发展建设市场研究报告.docx
