 《溶解度曲线》文档格式.docx
《溶解度曲线》文档格式.docx
- 文档编号:2955216
- 上传时间:2023-05-01
- 格式:DOCX
- 页数:60
- 大小:341.48KB
《溶解度曲线》文档格式.docx
《《溶解度曲线》文档格式.docx》由会员分享,可在线阅读,更多相关《《溶解度曲线》文档格式.docx(60页珍藏版)》请在冰点文库上搜索。
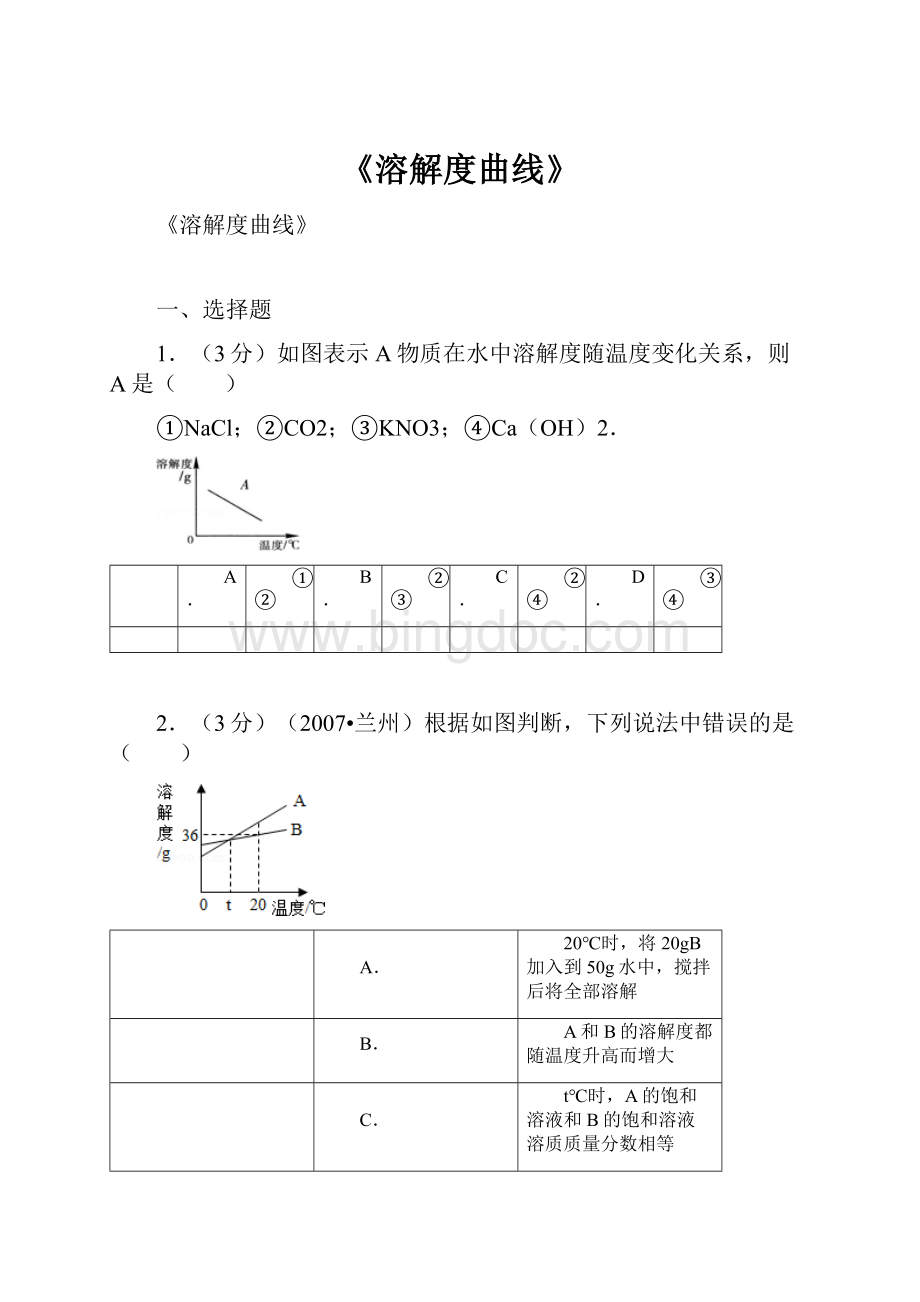
c一定是熟石灰的溶解度曲线
三种物质的饱和溶液分别从t2降温至t1℃,a、b析出的晶体质量相等
n点表示在t2℃时,a、b两种物质的饱和溶液溶质质量分数相同
4.(3分)如图是甲、乙、丙三种物质的溶解度曲线,下列说法正确的是( )
在t1℃时,三种物质的溶解度由大到小的顺序是甲>乙>丙
将一定质量的甲饱和溶液从t1℃升温到t2℃时,溶液中溶质质量分数不变
甲、乙、丙三种物质的饱和溶液升温都会转化为不饱和溶液
当乙的饱和溶液中混有少量丙时,可采用降温结晶的方法析出丙
5.(3分)(2010•盐城)如图是甲、乙两种固体物质的溶解度曲线,下列叙述不正确的是( )
甲、乙两种物质均属于易溶物质
甲物质的溶液度受温度变化影响较大
在20℃时,甲、两种物质的饱和溶液中溶质的质量相等
当甲中含有少量的乙时,可用降温结晶法提纯甲
6.(3分)如图为氯化铵和硫酸钠的溶解度曲线.下面说法中不正确的是( )
30℃时氯化铵和硫酸钠的饱和溶液的质量分数相同
40℃时硫酸钠的饱和溶液中溶质的质量分数最大
将50℃时硫酸钠的饱和溶液降低温度,始终有晶体析出
将60℃时硫酸钠的饱和溶液降温至40℃,溶质的质量分数不变
7.(3分)(2013•青岛二模)如图表示M、N两种固体物质的溶解度曲线,下列对图示信息的描述正确的是( )
30℃时M的溶解度小于N的溶解度
P点表示t℃时M、N的溶解度相等
M、N都是难溶物质
阴影处各点对应的溶液(不包含曲线上的点)是M的不饱和溶液,N的饱和溶液
8.(3分)(2011•贵港)t℃时,向10g水中逐渐加入硝酸钾晶体至饱和,则此过程中该溶液满足下图a、b两个变量的变化关系的是( )
a﹣溶解度,b﹣溶质质量
a﹣溶质的质量分数,b﹣溶质质量
a﹣溶质质量,b﹣溶剂质量
a﹣溶解度,b﹣溶剂质量
9.(3分)如图是A、B两种物质的溶解度曲线.在t1℃时往两个盛有100克水的烧杯中分别加入a克A物质和b克B物质,充分搅拌后都加热到t2℃.下列说法正确的是( )
t1℃时,AB两物质的溶解度相等.两杯溶液均是不饱和溶液
t1℃时,AB两物质的溶解度相等,A溶液为饱和溶液,B溶液为不饱和溶液
t2℃时,A的溶解度比B的溶解度大,两杯溶液均是不饱和溶液
t2℃时,A的溶解度比B的溶解度大,A溶液为不饱和溶液,B溶液为饱和溶液
10.(3分)(2009•咸宁)甲、乙两种固体纯净物的溶解度曲线如图1所示.在常温下,先在两支试管里分别装入甲、乙两种物质的饱和溶液(试管底部均有未溶解的固体),再放进盛有冰水的烧杯里(图2).下列说法正确的是( )
乙溶液中溶质的质量分数增大
装甲溶液的试管中剩余的固体减少
试管里甲、乙物质的溶解度都增大
两支试管里剩余的固体都增多
11.(3分)(2010•遵义)t1℃时,分别将20g甲、乙两种晶体(不含结晶水)加入盛有100g水的两个烧杯中,恰好完全溶解,升温到t2℃时出现甲、乙烧杯中所示的现象.根据上述实验,结合图中甲、乙两物质的溶解度曲线,判断下列说法正确的是( )
t1℃时烧杯中甲、乙两物质形成的溶液是不饱和溶液
t1℃时烧杯中甲、乙两物质形成的溶液溶质质量分数约为16.7%
t2℃时烧杯中甲物质溶液的质量是110g
t2℃时乙物质的溶解度是30g
12.(3分)根据M、N两种物质的溶解度曲线,往100g水中加入质量都是ag的M和N两种物质(假设两种物质的溶解性互不影响),制成t2温度下的混合物,将该混合物的温度降低到t1,下列说法不正确的是( )
t2温度下,得到的溶液中M已经饱和
t2温度下,得到的溶液中N已经饱和
温度降低到t1时,M和N两种物质的溶解度相等,溶液中两种物质均已饱和
温度降低到t1时,M和N两种物质的溶质质量分数相等,溶液中两种物质均不饱和
13.(3分)(2009•黄冈)如图为晶体M(不含结晶水)的溶解度曲线,a、b两点分别表示M物质的溶液.下列有关说法或a、b间的转化方法错误的是( )
t2℃时,a是饱和溶液,b是不饱和溶液
将两份溶液温度降到t1℃时,a、b中都有晶体析出
从a→b:
先将a降温到t1℃,过滤后将滤液升温到t2℃
从b→a:
在b中加入M至刚好饱和
14.(3分)(2008•烟台)如图是a、b两种物质的溶解度曲线.室温时,将盛有a、b饱和溶液的试管分别放入烧杯内的水中,均无晶体析出.当向烧杯内的水中加入硝酸铵固体或浓硫酸后,下图试管内所示现象正确的是( )
15.(3分)甲、乙的溶解度曲线如图,将t2℃甲、乙的饱和溶液分别降温到t1℃.下列说法一定正确的是( )
甲溶液仍饱和
两溶液仍饱和
溶质质量分数:
甲=乙
溶液质量:
二、非选择题
16.(4分)(2008•江西)如图,为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线.
(1)当温度为10℃时,碳酸钠的溶解度为 _________ ;
(2)当温度 _________ 时,氯化钠的溶解度大于碳酸钠的溶解度;
(3)生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”.
请你解释原因:
“夏天晒盐” _________ ;
“冬天捞碱” _________ .
17.(2分)(2003•江西)图为氯化钠和硝酸钾固体的溶解度曲线.根据该图可知:
氯化钠的溶解度受温度影响变化不大.此外由该图你还能获得的信息有:
(1) _________ .
(2) _________ .
18.(3分)(2010•宁德)图1是甲、乙、丙三种固体物质的溶解度曲线.根据图1、图2回答:
(1)50°
C时,甲、乙、丙三种固体物质的溶解度由大到小的顺序是 _________ .
(2)图2中,试管里预先装有少量生石灰,当往试管中加入适量水时,反应放出的热量使烧杯中某饱和溶液析出固体(不考虑水分蒸发).请判断:
该饱和溶液中的溶质是 _________ (填甲或乙或丙).
(3)从图1中,你能得到哪些信息?
_________ (任写一条).
19.(5分)(2010•桂林)A、B、C三种固体物质的溶解度曲线如图所示.
(1)t1℃时,A、B、C的溶解度大小关系是(用“>”、“<”或“=”表示) _________ ,它们的饱和溶液中,溶质质量分数最大的物质是 _________ .
(2)t2℃时,将A、B、C各25g分别放入100g水中,能形成饱
和溶液的物质是 _________ ,将其转化为不饱和溶液的两种
方法有 _________ 、 _________ .
20.(4分)(2006•河南)20℃时,分别将等质量的甲、乙两种固体物质加入到盛有10g水的两支试管中,充分溶解后,可观察到如图1所示的现象.20℃时 _________ (填“甲”或“乙”)物质的溶液一定是饱和溶液.图2表示的是甲、乙两种物质在水中的溶解度曲线.要使甲试管中的剩余固体继续溶解,可采用的方法有 _________ 、 _________ .
21.(6分)如图为A、B两种固体物质的溶解度曲线.
(1)Q点的含义是 _________ ;
(2)30℃时溶解30gA至少需要水的质量为 _________ g;
(3)30℃时配制A、B的饱和溶液各100g,需水较少的是 _________ .
22.(8分)(2010•兰州)右图是某实验小组的同学绘制的两种固体物质的溶解度曲线图.请你根据图示回答问题:
(1)t1℃时,a物质的溶解度 _________ b物质的溶解度(填“>”、“<”或“=”).
(2)将t2℃时a、b两种物质相同质量的饱和溶液,分别冷却到t1℃,析出晶体最多的是 _________ 物质.
(3)溶解度曲线图中的任何一点都表示溶液的一种特定状态.图中A、B两个状态中,溶液属于不饱和状态的是 _________ ,状态最不稳定的是 _________ .
23.(9分)如图是A、B两种物质的溶解度曲线,据图回答下列问题:
(1)当固体A中含有少量固体B时,可采用提纯A的方法是 _________ ;
(2)在30℃时 _________ (填“能”或“不能”)配制成30%的A溶液;
(3)在20℃,向100g5%的A溶液中加入5g水后,升高温度到30℃,需加入 _________ gA物质才能恰好饱和.
24.(6分)(2009•昆明)右图是某固体物质R的溶解度曲线,请根据图示回答下列问题:
(1)处于A点状态的R溶液当温度有t2变到t1时,其溶液中溶质质量分数将 _________ (填“变大”、“变小”或“不变”)
(2)处于B点状态的R溶液其它条件不变,当恒温蒸发溶剂时,B点的变动情况为下列选项的 _________ (填序号):
①向左平移②向右平移③向上平移④向下平移⑤保持不变
(3)将R的溶液B状态变到A状态,请设计并简述一个最简单的实验操作途径 _________ .
25.(8分)(2014•河北区一模)如图所示是甲、乙、丙三种物质的溶解度曲线,在20℃时,分别取等质量的三种物质的饱和溶液放入三只烧杯中,然后向溶液分别加入等质量的相应固体物质,再将温度升高到40℃,结果甲物质全部溶解,丙物质部分溶解,试回答下列问题:
(1)乙物质的溶解情况是 _________ ;
(2)依次写出甲、乙、丙三种物质的溶解度曲线的序号:
_________ ;
(用a、b、c填写)
(3)当温度在20℃~30℃时,三种物质的溶解度由大到小的顺序是 _________ ;
(用甲、乙、丙填空)
(4)40℃时,溶液中含水最少的是 _________ 物质.
26.(8分)(2010•上海)甲物质在水中的溶解度曲线如图,a、b、c、d为图象中的四个点.
①t1℃时,甲物质的溶解度是 _________ g/100g水.
②t2℃时,25g水中最多能溶解甲物质 _________ g.
③要使甲物质的饱和溶液成为不饱和溶液,可采用的一种方法是 _________ .
④甲物质的溶液分别处于a、b、c、d四个点时,溶液中甲的质量分
数大小关系正确的是 _________ (选填下列编号).
Ⅰ.c>d=b>aⅡ.c=d>a=bⅢ.c>a>b=dⅣ.c>a=b>d.
27.(12分)(2009•苏州)a.根据氢氧化钙的溶解度曲线,完成下列问题.
(1)曲线上满足A点指标的溶液在升高温度后会产生的现象是:
_________ ,此时的溶液中溶质质量分数将 _________ (选填“变大”或“变小”或“不变”)
(2)若向曲线上满足A点指标的溶液中加入生石灰,则溶液中的溶质质量将 _________ (选填“增加”或“减少”或“不变”)
b.根据氯化钠的溶解度曲线,完成下列问题.
(1)A点所示溶液为某温度下氯化钠的 _________ (选填“饱和”或“不饱和”)溶液.
(2)将B点所示的溶液升高温度到40℃(忽略水的蒸发),此时溶液中溶质质量分数将 _________ (选填“变大”或“变小”或“不变”).
(3)B点代表20℃时氯化钠的溶解度为36.0g,若将满足B点指标的溶液恒温蒸发10g水,会有 _________ g氯化钠晶体折出.
参考答案与试题解析
考点:
固体溶解度曲线及其作用.菁优网版权所有
专题:
溶液、浊液与溶解度.
分析:
根据各物质的溶解度随温度变化情况分析解答,氢氧化钙、气体的溶解度随温度的升高而降低,图示A物质的溶解度随温度升高而减小,据此分析解答.
解答:
解:
由图可知:
A物质在水中溶解度随温度的升高而减小,而NaCl的溶解度受温度影响不大;
CO2的溶解度随温度升高而减小;
KNO3;
的溶解度随温度的升高而增大;
Ca(OH)2的溶解度随温度升高而减小;
所以A可能是氢氧化钙和二氧化碳;
故选C.
点评:
了解常见固体和气体物质的溶解度随温度的变化情况即可顺利解答.
固体溶解度曲线及其作用;
溶质的质量分数、溶解性和溶解度的关系.菁优网版权所有
A、据该温度下B的溶解度分析解答;
B、据溶解度曲线可知物质的溶解度随温度变化情况;
C、一定温度下饱和溶液中溶解度相等,则溶质的质量分数相等;
D、A的溶解度随温度的降低而减小,据此分析解答.
A、20℃时B的溶解度是36g,所以将20gB加入到50g水中,不能全部溶解,最多溶解18g,故错误;
B、由图可知:
A、B的溶解度均随温度的升高而增大,正确;
C、饱和时溶质的质量分数=
×
100%,而t℃时二者的溶解度相等,所以A的饱和溶液和B的饱和溶液溶质质量分数相等,正确;
D、A的溶解度随温度的降低而减小,所以将将20℃时A的饱和溶液降温到0℃,会析出晶体,溶质的质量减小,溶剂的质量不变,所以溶质的质量分数减小,正确;
故选:
了解溶解度概念、溶解度曲线的意义,饱和溶液中溶质的质量分数的计算方法即可顺利解答.
固体溶解度的影响因素;
课本知识同类信息.
利用物质的溶解度曲线,判断与三种物质有关的说法是否正确,选出正确的一项.
A、a与b两溶解度曲线相交于一点,此时两物质的溶解度相等;
因此该说法不正确;
B、c曲线表示物质溶解度随温度升高而减小,虽然熟石灰溶解度也是随温度升高而减小,但并不是只有熟石灰是这种情况,气体物质的溶解度都随温度升高而减小.该选项说法不正确;
C、三种物质的饱和溶液分别从t2降温至t1℃,a、b两物质的溶解度变化量并不相等,因此析出的晶体质量也可能是不相等的;
D、n点为了a、b两物质在t2℃时的交点,此时,两物质的溶解度相等,则a、b两种物质的饱和溶液溶质质量分数相同;
故选D
一定温度饱和溶液中溶质的质量分数=
100%,因此,溶解度相同时饱和溶液的溶质质量分数相等.
结晶的原理、方法及其应用;
饱和溶液和不饱和溶液相互转变的方法.菁优网版权所有
A、据溶解度曲线可比较同一温度下不同物质的溶解度大小;
B、甲的溶解度随温度升高而增大,据此分析解答;
C、据物质的溶解度随温度升高的变化情况及饱和溶液、不饱和溶液的相互转化方法分析解答;
D、据二者的溶解度受温度影响情况分析提纯物质的方法.
A、在t1℃时,三种物质的溶解度由大到小的顺序是乙>甲>丙,故错误;
B、甲的溶解度随温度升高而增大,所以将一定质量的甲饱和溶液从t1℃升温到t2℃时,溶液中溶质、溶剂的质量不变,则溶质质量分数不变,正确;
C、甲乙的溶解度随温度升高而增大,升温其饱和溶液可变为不饱和溶液,丙的溶解度随温度升高而减小,升温析出晶体,依然是饱和溶液,故错误;
D、乙的溶解度随温度升高而增大,丙的溶解度随温度升高而减小,所以当乙的饱和溶液中混入丙,应采用蒸发结晶的方法析出丙,故错误;
故选B.
了解溶解度曲线的意义、提纯物质的方法,溶质的质量分数随溶解度的变化,才能结合题意灵活分析解答.
溶液、溶质和溶剂的相互关系与判断;
结合课本知识的信息.
根据固体的溶解度曲线可以:
①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
A、在20℃时,两种物质的溶解度相等是30g,大于10g,都是易溶物质,故A正确;
B、由两物质的溶解度曲线不难看出,甲的溶解度受温度的影响较大,故B正确;
C、在20℃时,两物质的溶解度相等,说明两物质的饱和溶液中溶质的质量分数相等,而不能是溶质质量相等,故C错误;
D、由于甲的溶解度随温度的升高而明显增大,而乙的溶解度受温度的影响较小,因此可以通过降温结晶的方法来提纯甲,故D正确;
本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.
晶体和结晶的概念与现象;
A、30℃时氯化铵和硫酸钠的溶解度相等,据饱和溶液中溶质的质量分数=
100%可知溶解度相等则溶质的质量分数相等;
B、一定温度下的饱和溶液中溶解度大则溶质的质量分数大;
C、据硫酸钠的溶解度随温度变化分析解答;
D、60℃降温至40℃,硫酸钠的溶解度逐渐增大,据此分析解答.
A、30℃时氯化铵和硫酸钠的溶解度相等,据饱和溶液中溶质的质量分数可知:
溶解度相等则饱和溶液中溶质的质量分数相等,正确;
40℃时硫酸钠的溶解度最大,所以硫酸钠饱和溶液中溶质的质量分数在该温度时最大,正确;
C、观察溶解度曲线可知:
在50℃至40℃时硫酸钠的溶解度随温度降低而增大,降温不会析出晶体,再继续降温,饱和溶液才晶体,故描述错误;
D、60℃降温至40℃,硫酸钠的溶解度逐渐增大,所以在该温度内饱和溶液降温不会析出晶体,溶质不变、溶剂不变,则溶质的质量分数不变,正确;
了解溶解度曲线的意义、饱和溶液中溶质的质量分数的计算方法,并能结合物质的溶解度变化曲线灵活分析解答问题.
物质的溶解性及影响溶解性的因素.菁优网版权所有
根据固体物质的溶解度曲线可知:
①查出某物质在一定温度下的溶解度,从而可以判断出物质的溶解性,②比较不同物质在同一温度下的溶解度大小,③判断出某点所代表的溶液是否饱和等.
A、由M、N两种固体物质的溶解度曲线可知,在30℃时,M的溶解度大于N的溶解度,故A错误;
B、由M、N两种固体物质的溶解度曲线可知,在t℃时,两物质的溶解度曲线交于P点,即两物质的溶解度相等,故B正确;
C、由M、N两种固体物质的溶解度曲线可知,在20℃时,两物质的溶解度都大于10g,故都属于易溶
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 溶解度曲线 溶解度 曲线
 冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 整编新型生态农业旅游休闲农庄项目发展建设市场研究报告.docx
整编新型生态农业旅游休闲农庄项目发展建设市场研究报告.docx
