 (浙江选考)2019版高考化学-考前提升训练11-电化学原理及其应用.doc
(浙江选考)2019版高考化学-考前提升训练11-电化学原理及其应用.doc
- 文档编号:16102828
- 上传时间:2023-07-10
- 格式:DOC
- 页数:7
- 大小:807.75KB
(浙江选考)2019版高考化学-考前提升训练11-电化学原理及其应用.doc
《(浙江选考)2019版高考化学-考前提升训练11-电化学原理及其应用.doc》由会员分享,可在线阅读,更多相关《(浙江选考)2019版高考化学-考前提升训练11-电化学原理及其应用.doc(7页珍藏版)》请在冰点文库上搜索。
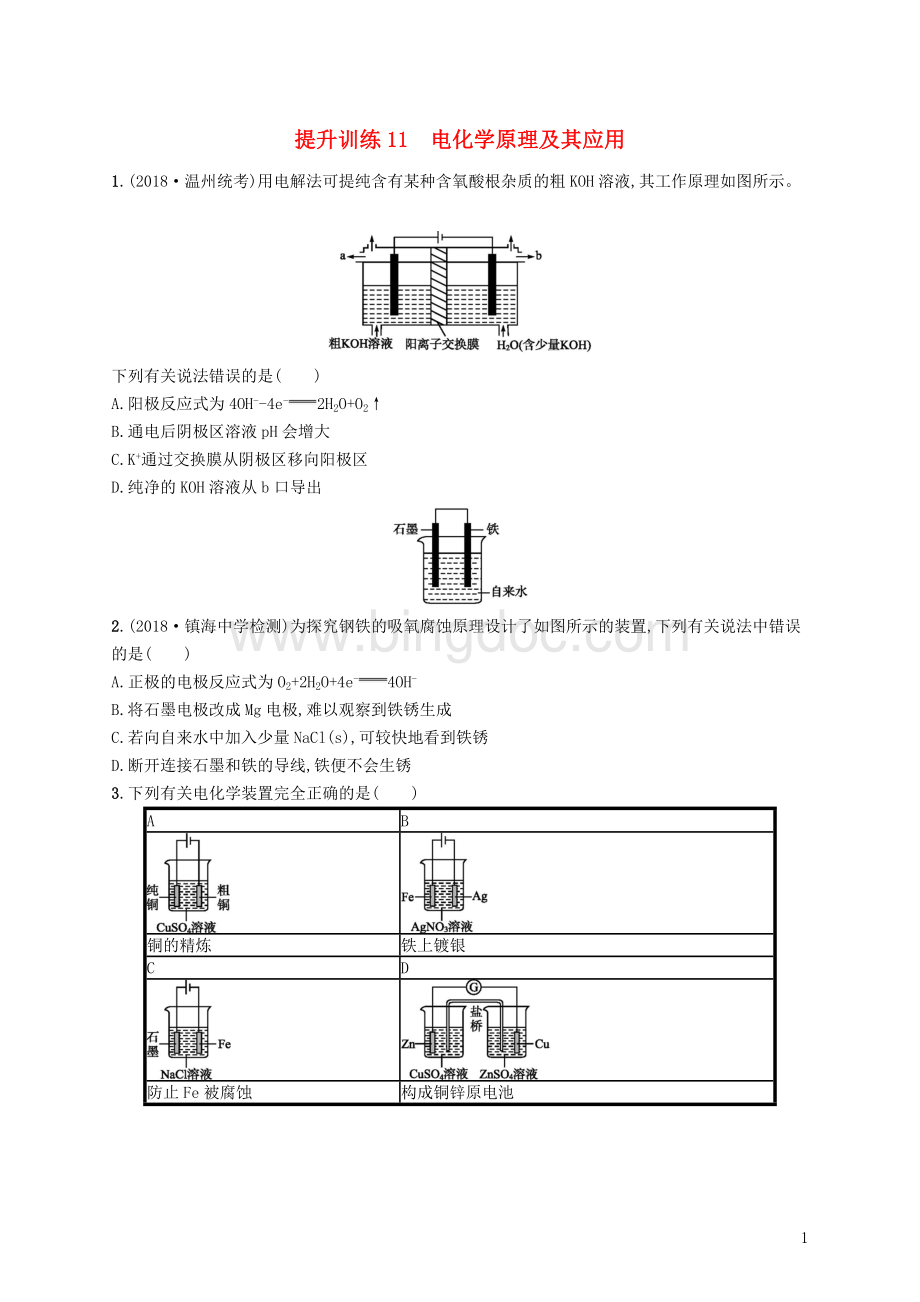
提升训练11 电化学原理及其应用
1.(2018·温州统考)用电解法可提纯含有某种含氧酸根杂质的粗KOH溶液,其工作原理如图所示。
下列有关说法错误的是( )
A.阳极反应式为4OH--4e-2H2O+O2↑
B.通电后阴极区溶液pH会增大
C.K+通过交换膜从阴极区移向阳极区
D.纯净的KOH溶液从b口导出
2.(2018·镇海中学检测)为探究钢铁的吸氧腐蚀原理设计了如图所示的装置,下列有关说法中错误的是( )
A.正极的电极反应式为O2+2H2O+4e-4OH-
B.将石墨电极改成Mg电极,难以观察到铁锈生成
C.若向自来水中加入少量NaCl(s),可较快地看到铁锈
D.断开连接石墨和铁的导线,铁便不会生锈
3.下列有关电化学装置完全正确的是( )
A
B
铜的精炼
铁上镀银
C
D
防止Fe被腐蚀
构成铜锌原电池
4.(2018·严州中学模拟)高铁酸盐在能源、环保等方面有着广泛的用途。
高铁酸钾(K2FeO4)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。
如图是高铁电池的模拟实验装置,下列说法不正确的是( )
A.该电池放电时正极的电极反应式为Fe+4H2O+3e-Fe(OH)3+5OH-
B.若维持电流强度为1A,电池工作10min,理论上消耗0.2gZn(已知F=96500C·mol-1)
C.盐桥中盛有饱和KCl溶液,此盐桥中氯离子向右池移动
D.若用阳离子交换膜代替盐桥,则钾离子向右移动
5.下列各组中,每种电解质溶液在惰性电极条件下电解时只生成氢气和氧气的是( )
A.HCl、CuCl2、Ba(OH)2 B.NaOH、CuSO4、H2SO4
C.NaOH、H2SO4、Ba(OH)2 D.NaBr、H2SO4、Ba(OH)2
6.(2018·普陀中学检测)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨),下列说法不正确的是( )
A.图中a极要连接电源的负极
B.C口流出的物质是硫酸
C.S放电的电极反应式为S-2e-+H2OS+2H+
D.B口附近溶液的碱性减弱
7.(2018·浙江十校联考)最近一家瑞典公司发明了一种新型充电器“PowerTrekk”,仅仅需要一勺水,它便可以产生维持10小时手机使用的电量。
其反应原理为Na4Si+5H2O2NaOH+Na2SiO3+4H2↑,则下列说法正确的是( )
A.该电池可用晶体硅作电极材料
B.Na4Si在电池的负极发生还原反应,生成Na2SiO3
C.电池正极发生的反应为2H2O+2e-H2↑+2OH-
D.当电池转移0.2mol电子时,可生成标准状况下1.12LH2
8.一种用于驱动潜艇的液氨—液氧燃料电池的工作原理示意如图,下列有关该电池说法正确的是( )
A.该电池工作时,每消耗22.4LNH3转移3mol电子
B.电子由电极A经外电路流向电极B
C.电池工作时,OH-向电极B移动
D.电极B上发生的电极反应为:
O2+4H++4e-2H2O
9.(2018·衢州检测)某手机电池采用了石墨烯电池,可充电5分钟,通话2小时。
一种石墨烯锂硫电池(2Li+S8Li2S8)工作原理示意图如图所示。
已知参与电极反应的单位质量的电极材料放出电能的大小称为该电池的比能量。
下列有关该电池说法不正确的是( )
石墨烯锂硫电池示意图
A.金属锂是碱金属中比能量最高的电极材料
B.A电极为该电源的负极,发生氧化反应
C.B电极的电极反应式:
2Li++S8+2e-Li2S8
D.电子从A电极经过外电路流向B电极,再经过电解质流回A电极
10.某小组同学用如图所示装置研究电化学原理。
下列关于该原电池的说法不正确的是( )
A.原电池的总反应为Fe+Cu2+Fe2++Cu
B.盐桥中是KNO3溶液,则盐桥中N移向乙烧杯
C.其他条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极反应式为2H++2e-H2↑
D.反应前,电极质量相等,一段时间后,两电极质量相差12g,导线中通过0.2mol电子
11.500mLKNO3和Cu(NO3)2的混合溶液中c(N)为6.0mol·L-1,用石墨电极电解此溶液,当通电一段时间后,两极均收到22.4L气体(标准状况),假定电解后溶液体积仍为500mL,下列说法正确的是( )
A.原混合溶液中c(K+)为4mol·L-1
B.电解后加入1molCu(OH)2可使溶液复原
C.电解后溶液中c(H+)为8mol·L-1
D.原溶液中c(Cu2+)为1mol·L-1
12.CH4可用于设计燃料电池,甲烷燃料电池的工作原理如图所示:
原电池工作过程中OH-的作用是 ;负极电极反应式为 。
若电路中转移电子数为0.8NA,左侧溶液pH (填“增大”“减小”或“不变”)(忽略溶液体积的变化),右侧的OH-物质的量变化量为 。
13.Ⅰ.钢铁的电化学腐蚀原理,在酸性环境中发生析氢腐蚀,在中性或碱性环境中发生吸氧腐蚀。
(1)写出图中石墨电极的电极反应式:
。
(2)将该装置作简单修改即可成为钢铁电化学防护的装置,请在图中虚线框内所示位置作出修改,并用箭头标出导线中电子移动方向。
Ⅱ.电化学原理在化学工业中有广泛的应用,请根据如图回答问题。
(1)装置A中的Y电极为 极,X电极的电极反应式为 ,工作一段时间后,电解质溶液的pH将 (填“增大”“减小”或“不变”)。
(2)若装置B中a为石墨电极、b为铁电极,W为饱和食盐水(滴有几滴酚酞溶液),则铁电极的电极反应式为
。
电解一段时间后若要恢复原溶液的成分和浓度,应该采用 的办法。
(3)若利用装置B进行铜的精炼,则a电极的材料为 ,工作一段时间后装置B电解液中c(Cu2+)将 (填“增大”“减小”或“不变”)。
(4)若装置B中a为Ag棒,b为铜棒,W为AgNO3溶液,工作一段时间后发现铜棒增重2.16g,则流经电路的电子的物质的量为 。
参考答案
提升训练11 电化学原理及其应用
1.C A项,阳极OH-放电,正确;B项,阴极电极反应式为2H++2e-H2↑,故c(OH-)增大,pH增大,正确;C项,电解时阳离子移向阴极,错误;D项,阳极区的K+透过阳离子交换膜移向阴极区,与阴极区的OH-结合成KOH,正确。
2.D A项,吸氧腐蚀的正极反应式为O2+4e-+2H2O4OH-,正确;B项,若把石墨电极改为Mg电极,此时Mg作负极,铁不会失电子,不会有铁锈生成,正确;C项,若向自来水中加入少量NaCl(s),溶液中离子浓度增大,腐蚀变快,正确;D项,若断开连接石墨和铁的导线,因铁中含有杂质,仍会发生腐蚀,错误。
3.C A项,电解精炼铜时,应该用粗铜作阳极,纯铜作阴极,错误;B项,铁上镀银时,应该用银作阳极,铁作阴极,错误;C项,该项是外加电流的阴极保护法,正确;D项,铜锌原电池中,锌应插入ZnSO4溶液中,铜应插入CuSO4溶液中,错误。
4.D A项,根据电池装置,Zn作负极,C为正极,高铁酸钾的氧化性很强,正极上高铁酸钾发生还原反应生成Fe(OH)3,正极电极反应式为Fe+4H2O+3e-Fe(OH)3+5OH-,正确;B项,若维持电流强度为1A,电池工作10min,通过电子为,则理论上消耗Zn的质量为×65g·mol-1≈0.2g,正确;C项,盐桥中阴离子向负极移动,盐桥起的作用是使两个半电池连成一个通路,使两溶液保持电中性,起到平衡电荷、构成闭合回路的作用,放电时盐桥中氯离子向右池移动,正确;D项,用某种高分子材料制成阳离子交换膜代替盐桥,则钾离子向左移动,错误。
5.C 电解HCl溶液生成氢气和氯气,电解CuCl2溶液生成Cu和氯气,电解Ba(OH)2溶液生成氢气和氧气,故A不选;电解NaOH溶液生成氢气和氧气,电解CuSO4溶液生成Cu、氧气、硫酸,电解H2SO4溶液生成氢气和氧气,故B不选;电解NaOH溶液、H2SO4溶液、Ba(OH)2溶液,均只生成氢气和氧气,故C选;电解NaBr溶液生成溴、氢气、NaOH,电解H2SO4溶液生成氢气和氧气,电解Ba(OH)2溶液生成氢气和氧气,故D不选。
6.D 根据Na+、S的移向判断阴、阳极。
Na+移向阴极区,a极应接电源负极,b极应接电源正极,其电极反应式分别为
阳极:
S-2e-+H2OS+2H+
阴极:
2H2O+2e-H2↑+2OH-
所以从C口流出的是H2SO4,在阴极区由于水中的H+放电,破坏水的电离平衡,c(H+)减小,c(OH-)增大,生成NaOH,碱性增强,从B口流出的是浓度较大的NaOH溶液。
7.C 该电池工作时生成氢氧化钠溶液,而硅可以与氢氧化钠反应,所以不能用晶体硅作电极材料,A不正确;Na4Si在电池的负极发生氧化反应,B不正确;电池正极的电极反应式为2H2O+2e-H2↑+2OH-,C正确;当电池转移0.2mol电子时,可生成标准状况下2.24LH2,D不正确。
8.B 温度、压强未知,无法计算22.4LNH3的物质的量,A错误;该电池中通入氧气的电极B为正极,电极A为负极,电子由电极A经外电路流向电极B,B正确;电池工作时,OH-向负极移动,C错误;该电池电解质溶液显碱性,电极B上发生的电极反应为O2+2H2O+4e-4OH-,D错误。
9.D 石墨烯锂硫电池的电极总反应式为2Li+S8Li2S8,Li失电子发生氧化反应,Li是负极材料。
A项,金属锂的摩尔质量小,单位质量的Li放出电能明显比其他碱金属大,正确;B项,电池内部阳离子向正极移动,则A电极为该电源的负极,发生氧化反应,正确;C项,B为电源的正极,发生的电极反应式为2Li++S8+2e-Li2S8,正确;D项,原电池的外电路中有电子转移,而电池的内部只有阴、阳离子的移动,没有电子的移动,错误。
10.B A项,根据图示可知,在该原电池中,负极是Fe,电极反应式为Fe-2e-Fe2+,石墨为正极,正极上的电极反应式为Cu2++2e-Cu,正、负极电极反应式相加得Fe+Cu2+Fe2++Cu,正确;B项,盐桥中是KNO3溶液,则根据同种电荷相互排斥,异种电荷相互吸引的原则,盐桥中N移向正电荷较多的甲烧杯,错误;C项,其他条件不变,若将CuCl2溶液换为NH4Cl溶液,由于溶液中阳离子获得电子的能力:
H+>N,石墨电极上的正极反应式为2H++2e-H2↑,正确;D项,反应前,电极质量相等,由于阳极发生反应Fe-2e-Fe2+,每转移2mol电子,负极减少质量56g,在正极发生反应Cu2++2e-Cu,质量增加64g,两个电极质量相差120g,则电解一段时间后,两电极质量相差12g,则导线中通过电子的物质的量为(12÷120)×2mol=0.2mol,正确。
11.B 电解KNO3和Cu(NO3)2的混合溶液,阳极上的电极反应式:
4OH--4e2H2O+O2↑,当产生22.4L即1mol(标准状况)氧气时,转移电子4mol,阴极上先发生电极反应:
Cu2++2e-Cu,然后是:
2H++2e-H2↑,在阴极上生成1mol氢气时,转移电子是2mol,所以铜离子共得到2mol电子,所以铜离子的物质的量为1mol,c(Cu2+)=2mol·L-1。
根据c(Cu2+)=2mol·L-1,可知Cu(NO3)2的浓度是2mol·L-1,其中的c(N)=4.0mol·L-1,又因原混合溶液中c(N)=6.0mol·L-1,所以原混合溶液中硝酸钾的浓度是2mol·L-1,所以c(K+)为2mol·L-1,A错误;根据出来什么补什么的原则,电解产物是1molCu、1molO2和1molH2,相当于1molCu(OH)2的组成,电解后加入1molCu(OH)2可使溶液复原,B正确;阳极上的电极反应式:
4OH--4e-2H2O+O2↑,当产生22.4L即1mol(标准状况)氧气时,转移电子4mol,消耗氢氧根离子4mol,阴极上发生了电极反应2H++2e-H2↑,在阴极上生成1mol氢气时,转移电子2mol,消耗氢离子2mol,所以电解后溶液中,如果忽略体积变化,则c(H+)==4mol·L-1,C错误;结合分析可知原溶液里c(Cu2+)=2mol·L-1,D错误。
12.答案:
参与电极反应,定向移动形成电流 CH4-8e-+10OH-C+7H2O 不变 0.2mol
解析:
甲烷失去电子转化为CO2,CO2结合氢氧根生成碳酸根,则氢氧根的作用是参与电极反应,定向移动形成电流;负极通入甲烷,电极反应式为CH4-8e-+10OH-C+7H2O。
若电路中转移电子数为0.8NA,正极消耗氧气0.2mol,生成氢氧根0.8mol,由于生成的氢氧根向负极移动,所以左侧溶液pH不变。
根据负极电极反应式可知右侧甲烷消耗1mol氢氧根,所以右侧的OH-物质的量变化量为1mol-0.8mol=0.2mol。
13.答案:
Ⅰ.
(1)O2+2H2O+4e-4OH-
(2)
Ⅱ.
(1)正 H2+2OH--2e-2H2O 减小
(2)2H++2e-H2↑ 通入适量HCl
(3)粗铜 减小
(4)0.02mol
解析:
Ⅰ.
(1)电解质溶液为NaCl溶液,呈中性,钢铁发生吸氧腐蚀。
负极上铁失电子发生氧化反应,正极上氧气得电子发生还原反应,电极反应式为O2+2H2O+4e-4OH-。
(2)Fe作电解池的阴极可被保护,所以给该装置加外接电源,应使负极与铁相连,电子从电源的负极流向铁,其图为。
Ⅱ.
(1)装置A为氢氧燃料电池,燃料在负极发生氧化反应:
H2+2OH--2e-2H2O;因反应消耗OH-且生成水,导致电解质溶液pH减小。
(2)根据图知,Y是正极,b是阴极,电解饱和食盐水时,阴极上氢离子放电生成氢气:
2H++2e-H2↑,因为电解过程中放出氢气和氯气,所以要恢复原溶液的成分和浓度,应通入适量的HCl。
(3)电解法精炼铜时,粗铜为阳极,精铜为阴极,所以阳极材料是粗铜;阳极上失电子变成离子进入溶液,因作阳极的粗铜中的铜和比铜活泼的金属都失去电子进入溶液,阴极溶液中Cu2+得到电子沉积在阴极上,所以,电解一段时间后,溶液中铜离子浓度减小。
(4)构成的装置为电镀装置,铜棒增重2.16g,为析出Ag的质量,则n(Ag)==0.02mol,故流经电路的电子的物质的量为0.02mol。
中华是礼仪之邦,礼是中国文化之心。
流传至今的儒家“十三经”中有三部礼学经典,习称“三礼”,一部是《仪礼》,记述周代冠、婚、丧、祭诸礼的仪式;另一部是《周礼》,记载理想国的官制体系;还有一部就是《礼记》,是孔门七十子后学阐发礼义的文集,凡四十九篇,虽以思想隽永、说理宏通见长,但亦不乏细节描述。
《礼记》全书主要有语录、条记、议论等形式,内容贴近生活,文字相对浅近。
今人读《礼记》,至少可以收获礼仪规范。
礼在社会生活层面属于行为规范,因而具有鲜明的可操作性的特点。
《礼记》记载了许多言谈举止方面的细节,尽管时代不同了,但其中不少内容依然可以继承。
例如《礼记》提到礼仪场合中的仪容仪态时说,“足容重”,步履要稳重;“手容恭”,拱手要高而端正;“目容端”,目光不可睇视;“口容止”,嘴形静止不妄动;“声容静”,不咳嗽、打喷嚏,哕咳;“头容直”,头部正直,不左右倾斜;“气容肃”,不喘大气;“色容庄”,神色庄重。
《礼记》还提及各种礼仪禁忌,如“毋嗷应”,不要用号呼之声回应对方的呼唤;“毋怠荒”,体态要整肃,不可懈怠;“坐毋箕”,坐着,不可将双腿向两侧张开;“暑毋褰裳”,即使是暑天,也不要将裳的下摆向上撩起。
这些都是文明时代民众必备的知识。
如何得体地访客、与尊长相处,也是《礼记》多次谈到的内容。
《礼记》说:
“将上堂,声必扬。
户外有二屦,言闻则入,言不闻则不入。
”拜访他人,即将上堂时,要抬高说话声,旨在使室内的主人知道客人已到,而有所准备。
如果房门口有两双鞋,房内的说话声清晰可闻,就可以进去;如果说话声听不到,说明他们的谈论比较私密,此时不可贸然进入。
《礼记》还说“毋侧听”,就是不要耳朵贴墙偷听别人谈话,这样做很不道德,可见古人把尊重他人隐私作为做人的原则。
《礼记》还屡屡谈及在尊长身旁陪坐时的注意事项,如:
“长者不及,毋儳言”,长者还没有谈及的话题,不要插嘴;“正尔容,听必恭”,听长者说话,要端正容貌,虚心恭听;“毋剿说,毋雷同”,自己发言时,要表达主见,不要总是袭用别人的说法,处处与人雷同。
《礼记》还说,在先生身旁陪坐,“先生问焉,终则对”,先生有所询问,要等先生说完后再回话,抢答是失礼的行为。
“请业则起,请益则起”,向先生请教学业,或者没听懂,希望先生再说一遍(请益),都要起身,不能坐着,以示尊师重道。
《礼记》中有许多格言,立意深刻,堪称人生准则,是引领人们修身进德、勉为君子的指南,而又朗朗上口,读之令人眼睛一亮,足以铭之左右,终身拳拳服膺。
在中国传统文化中,“礼”是内涵最大的概念,相当于西方人所说的“文化”,体系相当庞大,许多人对此不能理解,如果你读过《礼记》,就不会再有疑虑。
若逐篇细读,如网在纲,有条不紊,有助于从源头上把握中国文化体系。
(节选自《光明日报》,有删改)
1.下列关于《礼记》的表述,不符合原文意思的一项是(3分)
A.《礼记》是流传至今的儒家“十三经”中的三部礼学经典之一,另外两部,分别是《仪礼》和《周礼》。
B.《礼记》是一部阐发礼义的文集,总共有四十九篇,并非一人创作,而是孔门七十子后学的集体创作。
C.《礼记》一书思想内容隽永,说理宏通但不都是抽象枯燥空洞的议论,其中亦不乏具体的细节描述。
D.《礼记》全书都采用分条记述的语录体形式,以议论为主要表达方式,内容贴近生活,语言相对浅近。
2.根据原文内容,下列说法不正确的一项是(3分)
A.《礼记》对人们的手、足、目、口、头、声等各方面的仪容仪态都有详细而严格的要求,要求人们在礼仪场合要做到言行举止端庄文明。
B.按《礼记》的要求,拜访客人要有礼貌,不能贸然进屋,不能偷听别人的谈话,要尊重他人的隐私,这些做人的原则在当今仍有指导意义。
C.《礼记》鼓励人们发言要有主见,“毋剿说,毋雷同”,意即不要袭用别人的说法,观点不能与人雷同,提倡独立思考,发扬创新精神。
[.
D.《礼记》要求对尊长要谦恭尊重,听师长讲话要有耐心,不要随意插话,而且还要神态恭敬,请教尊长问题要起身,以示尊师重道。
3.下列理解和分析,不符合原文意思的一项是(3分)
A.虽然时代不同了,我们读《礼记》仍可学到一些社会生活中基本的行为规范,这些行为规范具有鲜明的可操作性。
B.读《礼记》我们可学到许多为人处世之道,以及待人接物应注意的事项,例如怎样在尊长旁陪坐,如何得体访客等。
C.读《礼记》可以学到许多让人受益终生的格言,这些格言立意深刻,引领人们修身进德,勉为君子,堪称人生准则。
D.读过《礼记》,就会发现“礼”在我国传统文化中是一个内涵最大的概念,就能够从源头上把握庞大的中国文化体系。
(二)文学类文本阅读(12分)
黄花渡
黄大刚
黄花渡是一个渡口,也是一座桥的名字。
黄花渡是黄家庄第一个大学生大林出资建造的。
28年后,大林从都市回到家乡时,看到黄花渡过往还是靠那只小木船摆渡,只不过那只小木船更破旧了,真不知道能不能载得动船上的重量。
大林的豪车只能望船兴叹。
大林很是气恼,还没进家门,先去找村长,“建一座桥需要多少钱,你说?
”
村长不知惊还是喜,半天答不上话来。
钱很快打到了村里的账户。
传出建桥的消息,兴奋喜悦的情绪在村子荡漾,村人说起这件事时,都说:
“这下好了……”黄老师也说:
“这下好了,学生上学不用划船了。
”
黄老师特意跑到集市给大林打电话。
“大林,”黄老师还像当年那样喊着他的名字,“你为家乡做了件大好事,老师以你为骄傲。
”
大林听了,嘴里客气着,心里却不以为然。
黄老师是大林的小学老师,那时候,大林去学校的路上有黄花溪,大林到黄花溪边就不走了,脱了洗衣服和小伙伴蹦进溪里玩,打水仗、捉鱼虾,玩饿了也不回家,摸进地里摘西瓜,挖地瓜,直到日落西山,才背着小书包,“放学”回家。
大林一天没到学校上学,黄老师紧跟其后家访。
大林正在埋头吃晚饭,黄老师说明来意,父亲一听今天没去上学,一把拉过还在低头吃饭的大林,巴掌立马扬得高高的。
黄老师忙把大林拽到身后,问:
“大林,今天怎么不去学校?
”
“我,我不敢过黄花溪。
”大林躲在黄老师身后,脖子一梗,答道。
黄老师一听,不再责怪大林,反而劝说他父亲,“福叔,孩子不懂事,慢慢教,大林是个不错的孩子,有前途的。
”
第二天,大林在父亲的催促下,背着书包去上学,才到黄花溪,就看见黄老师和那只小木船候在溪边。
大林只得乖乖上了船。
黄老师在船家的指点下,笨拙而吃力地把船撑到了对岸。
看黄老师手忙脚乱的样子,大林忍不住“噗”地笑出了声。
……
但大林玩心不改,总有这样的理由那样的借口逃课去玩,父亲打也打了,骂也骂了,无奈了最后吼一声:
“你要学就学,不学回家,老子给根牛绳让你牵。
”
一看父亲真动了脾气,大林也好像感到了事情的严重,不再说话,无助地看着前来家访的黄老师。
“学还是要上的,大林顽皮点,但聪明着呢,将来会有出息的。
”黄老师说。
在黄老师的劝说下,大林回到了学校。
黄老师经常对大林他们讲外面的世界。
在黄老师的描述下,大林他们露出了向往的神色,不由好奇地问这问那。
大林说:
“外面的世界有什么呢?
老师,你去过吗?
……”
黄老师说:
“外面的世界精彩着呢,单说省城,就有供人闲暇时放松心情的美丽的公园,还有你们喜欢的动物园,里面有老虎、大象、猴子……”
“还有什么呢?
”
“还有跑得比牛快的汽车,有像长蛇一样的火车,有飞机,有高到云端的大楼……”
“只要你们按时上学,认真学习,不逃学,有机会老师带你们去省城看看。
”
老师的话激起一片欢呼。
“你们要努力学习,走出这黄花渡。
”黄老师意味深长地说。
、
黄老师看着远方,脸上浮现出幸福的微笑,好像看到了孩子们的未来,看到了自己的梦想……
段考后,黄老师自掏腰包,带大林他们去了一趟省城。
大林梦想去动物园、公园玩,但黄老师带他们去的是省城的大学校园,从那一刻起,当一名大学生的念头像一颗种子在大林的心里发芽。
大林不仅如愿考上了大学生,还走向了外面精彩的世界。
多少年过去了,黄老师还留在黄家庄当老师,多年的乡村教师生涯,已把黄老师磨得与一个农民无异。
再想起黄老师当年鼓励自己走向外面精彩世界的话,大林突然觉得老师那些话语过于虚伪,要是真如老师讲的那样,那黄老师干嘛窝在黄家庄一辈子。
桥建好了,名字大林也想好了,就以捐资者的名字命名,这是惯例的,只是他不好意思提而已。
还没等大林找个合适的人来表达他的意思,父亲却提议以黄老师的名字命名这座桥,父亲说:
“黄老师是村里第一个走出黄花溪的人,可为了村里的孩子,又从外面精彩的世界回到了黄家庄。
”
还有这等事,多少年过去了,要不是父亲提起,他永远不知晓。
但黄老师说:
“不是已有现成的名字吗,就叫黄花渡吧。
”
4.黄老师有哪些性格特点?
请简要分析。
(4分)
5.小说采用插叙的手法交代大林儿时上学的表现有何作用?
(4分)
6.小说也以“黄花渡”为题,有何用意?
结合全文谈谈你的看法。
(4分)
(三)实用类文本阅读(12分)
阅读下面的文字,完成7~9题。
一代儒宗马一浮
郭继民
学者刘梦溪曾以“高人逸士”评价马一浮。
马一浮幼年时
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 浙江 2019 高考 化学 考前 提升 训练 11 电化学 原理 及其 应用
 冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 负债.pptx
负债.pptx
 高三教师年度考核个人工作总结5篇.docx
高三教师年度考核个人工作总结5篇.docx
