 高考化学真题和模拟类编专题13元素和化合物知识的综合应用.docx
高考化学真题和模拟类编专题13元素和化合物知识的综合应用.docx
- 文档编号:14797575
- 上传时间:2023-06-27
- 格式:DOCX
- 页数:21
- 大小:466.13KB
高考化学真题和模拟类编专题13元素和化合物知识的综合应用.docx
《高考化学真题和模拟类编专题13元素和化合物知识的综合应用.docx》由会员分享,可在线阅读,更多相关《高考化学真题和模拟类编专题13元素和化合物知识的综合应用.docx(21页珍藏版)》请在冰点文库上搜索。
高考化学真题和模拟类编专题13元素和化合物知识的综合应用
2018年高考试题,
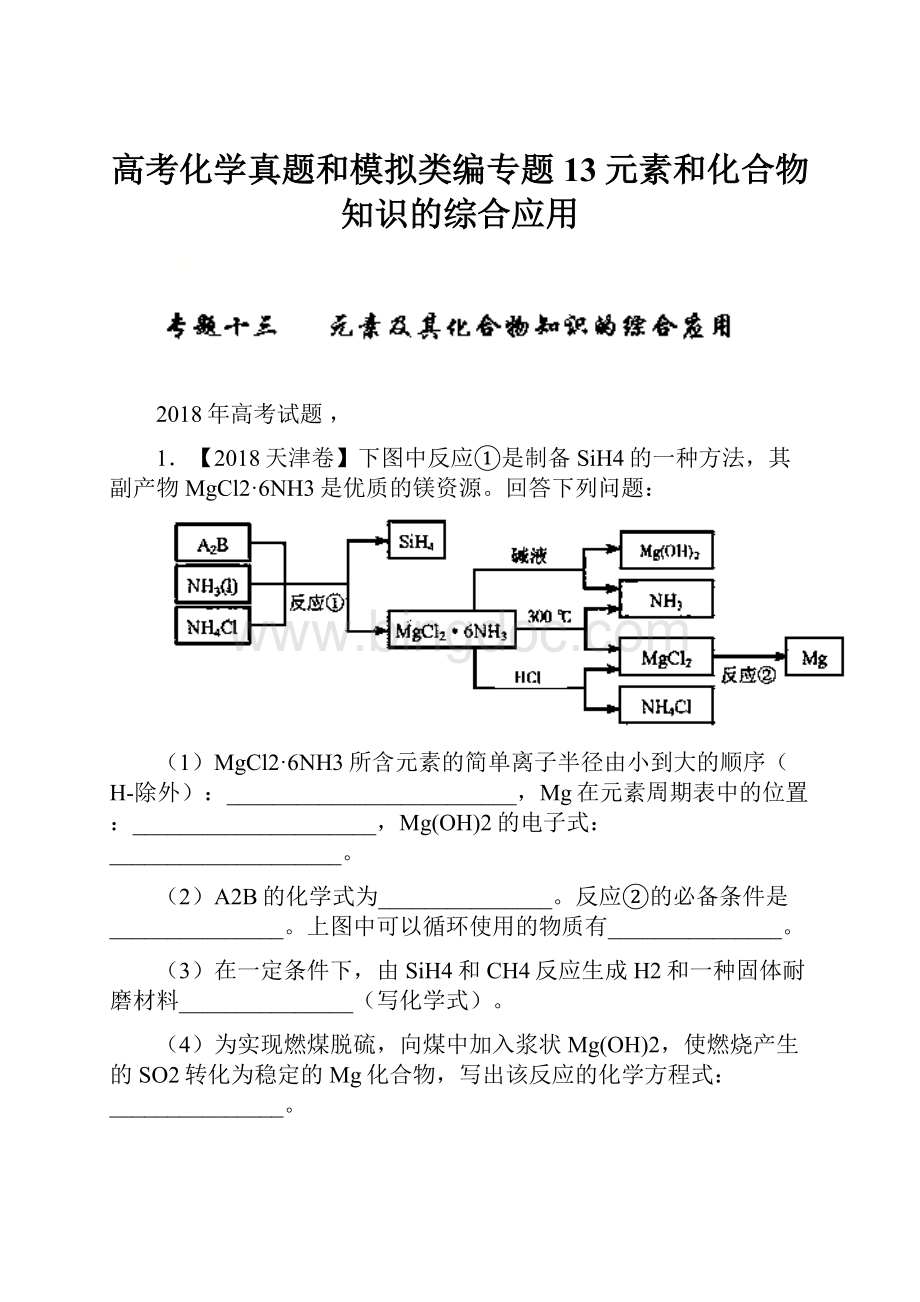
1.【2018天津卷】下图中反应①是制备SiH4的一种方法,其副产物MgCl2·6NH3是优质的镁资源。
回答下列问题:
(1)MgCl2·6NH3所含元素的简单离子半径由小到大的顺序(H-除外):
_________________________,Mg在元素周期表中的位置:
_____________________,Mg(OH)2的电子式:
____________________。
(2)A2B的化学式为_______________。
反应②的必备条件是_______________。
上图中可以循环使用的物质有_______________。
(3)在一定条件下,由SiH4和CH4反应生成H2和一种固体耐磨材料_______________(写化学式)。
(4)为实现燃煤脱硫,向煤中加入浆状Mg(OH)2,使燃烧产生的SO2转化为稳定的Mg化合物,写出该反应的化学方程式:
_______________。
(5)用Mg制成的格氏试剂(RMgBr)常用于有机合成,例如制备醇类化合物的合成路线如下:
依据上述信息,写出制备
所需醛的可能结构简式:
_______________。
【答案】r(H+) Mg2Si熔融,电解NH3,NH4ClSiC2Mg(OH)2+2SO2+O2=2MgSO4+2H2OCH3CH2CHO,CH3CHO 【解析】分析: 根据反应的流程过程,先判断出A2B的化学式,带入框图,结合学习过的相关知识进行分析即可。 详解: (1)MgCl2·6NH3所含元素的简单离子为Mg2+、Cl、N3-、H+,比较离子半径应该先看电子层,电子层多半径大,电子层相同时看核电荷数,核电荷数越大离子半径越小,所以这几种离子半径由小到大的顺序为: r(H+) Mg在周期表的第三周期ⅡA族。 氢氧化镁是离子化合物,其中含有1个Mg2+和2个OH-,所以电子式为: 。 (2)根据元素守恒,A2B中就一定有Mg和Si,考虑到各自化合价Mg为+2,Si为-4,所以化学式为Mg2Si。 反应②是MgCl2熔融电解得到单质Mg,所以必备条件为: 熔融、电解。 反应①需要的是Mg2Si、NH3和NH4Cl,而后续过程又得到了NH3和NH4Cl,所以可以循环的是NH3和NH4Cl。 (3)在一定条件下,由SiH4和CH4反应生成H2和一种固体耐磨材料,该耐磨材料一定有Si和C,考虑到课本中介绍了碳化硅的高硬度,所以该物质为SiC。 点睛: 本题是一道比较基本的元素综合问题,比较新颖的是在题目的最后一问中加入了一个有机小题,这样的无机有机综合题目是比较少见的,当然难度并不大。 第(4)小题中的反应,可以参考必修1的课后练习中涉及的钙基固硫问题。 方程式中按道理应该加上反应的条件,例如: 加热。 2.【2018江苏卷】碱式硫酸铝溶液可用于烟气脱硫。 室温下向一定浓度的硫酸铝溶液中加入一定量的碳酸钙粉末,反应后经过滤得到碱式硫酸铝溶液,反应方程式为(2−x)Al2(SO4)3+3xCaCO3+3xH2O 2[(1−x)Al2(SO4)3·xAl(OH)3]+3xCaSO4↓+3xCO2↑生成物(1−x)Al2(SO4)3·xAl(OH)3中x值的大小影响碱式硫酸铝溶液的脱硫效率。 (1)制备碱式硫酸铝溶液时,维持反应温度和反应时间不变,提高x值的方法有___________________。 (2)碱式硫酸铝溶液吸收SO2过程中,溶液的pH___________(填“增大”、“减小”、“不变”)。 (3)通过测定碱式硫酸铝溶液中相关离子的浓度确定x的值,测定方法如下: ①取碱式硫酸铝溶液25.00mL,加入盐酸酸化的过量BaCl2溶液充分反应,静置后过滤、洗涤,干燥至恒重,得固体2.3300g。 ②取碱式硫酸铝溶液2.50mL,稀释至25mL,加入0.1000mol·L−1EDTA标准溶液25.00mL,调节溶液pH约为4.2,煮沸,冷却后用0.08000mol·L−1CuSO4标准溶液滴定过量的EDTA至终点,消耗CuSO4标准溶液20.00mL(已知Al3+、Cu2+与EDTA反应的化学计量比均为1∶1)。 计算(1−x)Al2(SO4)3·xAl(OH)3中的x值(写出计算过程)。 【答案】 (1)适当增加CaCO3的量或加快搅拌速率 (2)减小 (3)25mL溶液中: n(SO42−)=n(BaSO4)= =0.0100mol 2.5mL溶液中: n(Al3+)=n(EDTA)−n(Cu2+)=0.1000mol·L−1×25.00mL×10−3L·mL−1−0.08000mol·L−1×20.00mL ×10−3L·mL−1=9.000×10−4mol 25mL溶液中: n(Al3+)=9.000×10−3mol 1mol(1−x)Al2(SO4)3·xAl(OH)3中 n(Al3+)=(2−x)mol;n(SO42−)=3(1−x)mol x=0.41 【解析】分析: (1)提高x的值,即促进Al3+的水解和CaSO4的生成。 (2)碱式硫酸铝溶液吸收SO2,溶液碱性减弱,pH减小。 (3)根据加入过量BaCl2溶液产生的固体计算n(SO42-);由消耗的CuSO4计算过量的EDTA,由Al3+消耗的EDTA计算n(Al3+);根据n(Al3+)与n(SO42-)之比计算x的值。 (3)25mL溶液中: n(SO42-)=n(BaSO4)= =0.0100mol 2.5mL溶液中: n(Al3+)=n(EDTA)−n(Cu2+)=0.1000mol·L−1×25.00mL×10−3L·mL−1−0.08000mol·L−1×20.00mL×10−3L·mL−1=9.000×10−4mol 25mL溶液中: n(Al3+)=9.000×10−3mol 1mol(1-x)Al2(SO4)3·xAl(OH)3中n(Al3+)=(2-x)mol;n(SO42-)=3(1-x)mol = = ,解得x=0.41。 点睛: 本题以碱式硫酸铝溶液的制备原理为背景,考查反应原理的理解、反应条件的控制和有关化学式的计算。 解题的关键有: ①向硫酸铝溶液中加入CaCO3生成碱式硫酸铝溶液,CaCO3的作用是调节pH促进Al3+水解,同时将SO42-转化为CaSO4沉淀;②理解溶液中的离子反应与实验滴定方法的定量计算,理清物质间的计量关系。 3.【2018届文山州毕业考】某小组探究Na2CO3和NaHCO3的性质,实验步骤及记录如下: Ⅰ.分别向盛有0.5gNa2CO3固体、0.5gNaHCO3固体的烧杯中加入10mL水(20℃),搅拌,测量温度为T1; Ⅱ.静置恒温后测量温度为T2; Ⅲ.分别加入10mL密度约为1.1g·mL-120%的盐酸(20℃),搅拌,测量温度T3。 得到下表1的数据: 回答下列问题: (1)Na2CO3溶于水显碱性,其原因是______________________(用离子方程式表示)。 (2)根据试题后的附表判断: 步骤Ⅰ中Na2CO3、NaHCO3固体分别是全部溶解还是部分溶解____________________________________。 (3)分析表1的数据得出: Na2CO3固体溶于水________,NaHCO3固体溶于水________(填“放热”或“吸热”)。 (4)甲同学分析上述数据得出: Na2CO3和NaHCO3与盐酸反应都是放热反应。 乙同学认为应该增加一个实验,并补做如下实验: 向盛有10mL水(20℃)的烧杯中加入10mL________,搅拌,测量温度为22.2℃。 (5)结合上述探究,下列说法正确的是________。 A.NaHCO3与盐酸的反应是吸热反应 B.不能用稀盐酸鉴别Na2CO3和NaHCO3固体 C.Na2CO3、NaHCO3固体与稀盐酸反应的能量变化还与物质的溶解等因素有关 (6)丙同学为测定一份NaHCO3和Na2CO3混合固体中NaHCO3的纯度,称取m1g混合物,加热至质量不变时,称其质量为m2g,则原混合物中NaHCO3的质量分数为________(用代数式表示)。 附表: 溶解度表 . 【答案】CO +H2O HCO +OH-Na2CO3和NaHCO3固体都是全部溶解放热吸热密度约为1.1g·mL-120%的盐酸(20℃)AC ×100% 【解析】 (1)碳酸钠为强碱弱酸盐,钠离子不水解、碳酸根离子水解导致溶液呈碱性,以第一步水解为主,水解离子方程式为: CO32-+H2O⇌HCO3-+OH-,故答案为: CO32-+H2O⇌HCO3-+OH-; (4)强酸溶于水放热,盐酸为强酸,所以需增加探究盐酸溶于水温度的变化,即10mL密度约为1.1g/mL20%的盐酸搅拌,测量温度为22.2℃,故答案为: 密度约为1.1g/mL20%的盐酸; (5)A.盐酸溶于水放热,测量温度为22.2℃,T1/℃,NaHCO3固体溶于水温度从20℃升高到18.5℃,吸热,两者反应恒温后测量温度T3为20.8℃低于22.2℃,所以NaHCO3与盐酸的反应是吸热反应,故A正确;B.用稀盐酸鉴别NaHCO3和Na2CO3溶液,反应较快的为NaHCO3,能鉴别,故B错误;C.从上述温度变化数值可判别Na2CO3、NaHCO3固体与稀盐酸反应的能量变化还与物质的溶解等因素有关,故C正确.故选AC; 4.【2018届盐城市三模】Ca10(PO4)6(OH)2(羟基磷酸钙,简写HAP)是一种新型的环境功能矿物材料,可用于除去水体中的F-、Cd2+、Pb2+ 及Cu2+等。 (1)制备HAP的步骤如下: 分别配制250mL浓度均为0.5mol·L-1的Ca(NO3)2溶液和(NH4)2HPO4溶液(pH约为8),按n(Ca)/n(P)=1.67分别量取相应体积的溶液,加热至50℃,不断搅拌下,按特定的方式加料,强力搅拌1h,再经后续处理得到产品。 ①特定的加料方式是__________(填序号)。 a.将Ca(NO3)2溶液逐滴滴入(NH4)2HPO4溶液中, 再用氨水调节pH至10.5 b.将(NH4)2HPO4溶液逐滴滴入Ca(NO3)2溶液中,再用氨水调节pH至10.5 c.将(NH4)2HPO4溶液和氨水混合并调节pH至10.5,再滴入Ca(NO3)2溶液 ②反应生成Ca10(PO4)6(OH)2的离子方程式为__________。 (2)HAP脱除F-的操作是: 在聚四氟乙烯烧杯中加入50mL 10mg·L-1NaF溶液和0.15gCa10(PO4)6(OH)2,在恒温下振荡,每隔1h测定一次溶液中F-浓度,直至达到吸附平衡。 ①实验中“烧杯”材质用“聚四氟乙烯”塑料而不用玻璃,其原因是__________。 ②除氟反应形式之一是: Ca10(PO4)6(OH)2+20F- 10CaF2+6PO43-+2OH-,该反应的平衡常数K=__________[用Ksp(CaF2)和Ksp(HAP)表示]。 (3)HAP脱除Pb(Ⅱ)包括物理吸附和溶解-沉淀吸附。 物理吸附时,HAP的特定位可吸附溶液中某些阳离子;溶解-沉淀吸附的机理为: Ca10(PO4)6(OH)2(s)+2H+(aq) 10Ca2+(aq)+6PO43-(aq)+2H2O(l)(溶解) 10Pb2+(aq)+6PO43-(aq)+2H2O(l) Pb10(PO4)6(OH)2(s)+2H+(aq)(沉淀) 已知Pb(Ⅱ)的分布分数如图-1所示;一定条件下HAP对Pb (1)平衡吸附量与pH的关系如图-2所示。 ①能使甲基橙显红色的Pb(Ⅱ)溶液中滴入少量NaOH至溶液呈中性,该过程中主要反应的离子方程式为__________。 ②当pH<3.0时,pH越小HAP对Pb(Ⅱ)平衡吸附量稍减小,其原因是__________。 ③当pH> 7.0时,生成的沉淀为__________(填化学式);此时pH越大HAP对Pb(Ⅱ)平衡吸附量越小,其原因是__________。 【答案】b10Ca2++6HPO42-+8NH3·H2O Ca10(PO4)6(OH)2↓+8NH4++6H2O防止F-及其水解生成的HF与玻璃中SiO2反应Ksp(HAP)/K10sp(CaF2)Pb2++OH-=Pb(OH)+溶液中c(H+)大,大量H+占据HAP 对Pb2+的吸附位,物理吸附能力减弱Pb10(PO4)6(OH)2 和Pb(OH)2c(H+)减小,会减少HAP 在溶液中的溶解量,便生成的c(PO43-)减小,溶解-沉淀吸附能力减弱且改变了吸附机理 5.【2018届红桥区二模】I.铁是生产、生活及生命中的重要元素。 (1)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。 NaNO2因具有氧化性能使血红蛋白丧失与O2结合能力。 药品美蓝是其有效的解毒剂,解毒时美蓝发生_____反 应(填“氧化”或“还原”)。 (2)现有一瓶放置了一段时间的某浓度的FeCl3溶液,请设计实验检验其中是否含有Fe3+_____。 (3)普通铁粉与水蒸气在高温下反应生成铁的某种氧化物和氢气,该氧化物和氢气在高温下发生逆反应得到“引火铁”。 若一定量的普通铁粉和水蒸气在高温下反应生成44.8LH2 (已换算到标况下),则转移电子数目为_______;“引火铁”是一种极细的铁粉,它在空气中可以自燃,其原因是_____________。 II.化合物M是某种具有磁学性质的新型电子材料的主要成分,由两种元素组成。 为了研究其组成,设计如下实验: 气体甲可使湿润红色石蕊试纸交蓝。 请回答: (1) M的化学式___________,气体甲的电子式__________。 (2)白色沉淀乙在空气中变成红褐色沉淀丙的原因是(用化学方程式表示)_______________。 (3) 高温条件下,丁与甲反应生成两种单质和水,该反应的化学方程式为______________。 【答案】氧化取少量待测液,滴加KSCN溶液,若溶液呈血红色,说明原溶液中有Fe3+,反之则没有4NA引火铁表而积很大,加快了与氧气反应速度Fe4N 4Fe(OH)2+O2+2H2O=4Fe(OH)3Fe2O3 +2NH3 2Fe +N2 +3H2O 【解析】I. (1)NaNO2因具有氧化性能使血红蛋白丧失与O2结合能力,原因是氧化了血红蛋白中的二价铁,药品美蓝是其有效的解毒剂,这说明该物质具有还原性,因此解毒时美蓝发生氧化反应;正确答案: 氧化。 (2)一般用硫氰化钾溶液检验铁离子,操作过程: 取少量待测液,滴加KSCN溶液,若溶液呈血红色,说明原溶液中有Fe3+,反之则没有;正确答案: 取少量待测液,滴加KSCN溶液,若溶液呈血红色,说明原溶液中有Fe3+,反之则没有。 (3)标况下44.8LH2,其物质的量为2mol,反应转移的电子数目为2×2×NA=4NA;引火铁表而积很大,加快了与氧气反应速度,因此在空气中可以自燃;正确答案: 4NA;引火铁表而积很大,加快了与氧气反应速度。 (2)白色沉淀乙是氢氧化亚铁,在空气中被氧气氧化为红褐色氢氧化铁,反应的化学方程式: 4Fe(OH)2+O2+2H2O=4Fe(OH)3;正确答案: 4Fe(OH)2+O2+2H2O=4Fe(OH)3。 (3) 高温条件下,氧化铁与氨气反应生成铁、氮气和水,该反应的化学方程式为: Fe2O3+2NH3 2Fe+N2+3H2O;正确答案: Fe2O3+2NH3 2Fe+N2+3H2O。 点睛: Fe(OH)2不稳定,易被氧气氧化为Fe(OH)3,所以Fe(OH)2在空气中迅速变为灰绿色,最终变为红褐色,据此现象作为进行物质的推断的一个题眼。 6.【2018届南通市三模】摩尔盐[(NH4)2Fe(SO4)2·6H2O]是一种重要的化工原料,可用于制取纳米Fe3O4和草酸合铁酸钾等。 (1)取一定质量摩尔盐样品与过量NaOH溶液反应。 ①根据生成气体的体积计算得到摩尔盐的纯度小于实际值,其原因是______。 ②向所得Fe(OH)2沉淀中加入NaNO2溶液可制得纳米Fe3O4,同时产生NO。 该反应的离子方程式为______。 (2)摩尔盐经氧化后与KOH和H2C2O4反应可得到草酸合铁酸钾[KaFeb(C2O4)c·dH2O],其中Fe元素化合价为+3。 ①已知25℃,H2C2O4的电离常数Ka1=5.6×10-2,Ka2=5.4×10-5。 pH=4的H2C2O4溶液中c(C2O ): c(HC2O )=______。 ②为了确定草酸合铁酸钾的组成,准确称取4.910g样品在氮气气氛下加热,固体样品的剩余质量随温度的变化如图所示。 已知: a.120℃时已完全失去结晶水。 b.200℃~580℃分解产生的CO和CO2恢复至标准状况下体积为1.008L。 c.580℃以上残留固体为FeO和K2CO3的混合物。 根据以上实验数据计算草酸合铁酸钾中的n(Fe3+): n(C2O42-)_____________(写出计算过程)。 【答案】氨气极易溶于水,溶液中有部分氨气没有逸出3Fe(OH)2+2NO =Fe3O4+2NO↑+2OH—+2H2O0.54根据元素守恒得到分解产生的气体为CO和CO2,n(CO)+n(CO2)= =4.5×10-2mol,2n(C2O42-)=n(K2CO3)+n(CO)+n(CO2)=n(K2CO3)+4.5×10-2mol,n(Fe3+)×72g·mol-1+ n(K+)×138g·mol-1=2.79g,3n(Fe3+)+n(K+)=2×[ n(K+)+4.5×10-2mol]× ,解得: n(Fe3+)=1×10-2moln(K+)=3×10-2mol,n(C2O42-)=3×10-2mol,n(Fe3+): n(C2O42-)=1×10-2mol: 3×10-2mol=1: 3 【解析】 (1)①摩尔盐[(NH4)2Fe(SO4)2·6H2O]与氢氧化钠反应生成氨气,氨气极易溶于水,溶液中有部分氨气没有逸出,因此根据生成气体的体积计算得到摩尔盐的纯度小于实际值,故答案为: 氨气极易溶于水,溶液中有部分氨气没有逸出; ②Fe(OH)2沉淀中加入NaNO2溶液可制得纳米Fe3O4,同时产生NO,反应的离子方程式为3Fe(OH)2+2NO2-=Fe3O4+2NO↑+2OH—+2H2O,故答案为: 3Fe(OH)2+2NO2-=Fe3O4+2NO↑+2OH—+2H2O; (2)①已知25℃,H2C2O4的电离常数Ka1=5.6×10-2,Ka2=5.4×10-5。 pH=4的H2C2O4溶液中 = = = =0.54,故答案为: 0.54; 7.【2018届宝山区二模】铝、铁是常见的两种金属,它们的单质及化合物在生活生产中处处可见。 (1)过量的铁和稀硝酸发生反应,产物是Fe(NO3)2和NO,写出该反应的化学方程式___________。 (2)实验室配制FeSO4溶液时,如果没有隔绝空气,FeSO4会被氧化为_______(填写化学式)。 在该溶液中加入___________试剂,看到_____________________现象,证明溶液变质。 (3)KAl(SO4)2·12H2O俗称明矾,常用作净水剂,请述其原因并写出有关的离子方程式____________________。 (4)已知Ba(AlO2)2可溶于水,下图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系。 由图可知c点的沉淀是________(填化学式),已知a-b时存在的沉淀是Al(OH)3和BaSO4,两者的物质的量: ________比________多。 【答案】3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2OFe2(SO4)3KSCN溶液溶液变为血红色明矾水解生成胶状Al(OH)3,它具有很强的吸附能力,可以吸附水中的杂质并沉降,使水澄清。 Al3++3H2O Al(OH)3+3H+BaSO4BaSO4Al(OH)3 点睛: 本题考查学生离子之间的反应知识,结合图象知识来考查,增加了难度,熟悉每一段图中对应的化学反应是解答本题的关键,根据整个过程中离子之间的反应以及用量来确定沉淀的量的多少。 8.【2018届陕西省二模】亚硝酸钠(化学式为NaNO2)是一种常用的防腐剂,回答下列问题: (1)NaNO2中N元素的化合价为_________. (2)亚硝酸钠在320°C时能分解产生氧化钠固体、一氧化氮和一种常见的助燃性气体。 该反应的化学方程式_________________。 (3)我国规定火腿肠中亚硝酸钠添加标准为每千克食品含量不超过150毫克,以此计算,200g15%的亚硝酸钠溶液至少可用于生产火腿肠______千克。 (4)在酸性条件下,NaNO2与按物质的量1: 1恰好完全反应,且I-被氧化为I2时,产物中含氮的物质为________(填化学式)。 (5)工业废水中的NaNO2可用铝粉除去,已知此体系中包含AI、NaAlO2、NaNO2、NaOH、NH3、H2O六种物质。 该反应的化学方程式为____________。 (6)某同学设计实验对工业产品中NaNO2的含量进行测定,你取固体样品2g,完全溶解配制成溶液100mL取出25mL溶液用0.100mol/L酸性KMnO4溶液进行滴定(杂质不与KMnO4反应),实验所得数据如下表所示: 滴定次数 1 2 3 4 消耗KMnO4溶液体积/mL 20.70 20.02 20.00 19.98 该样品中亚硝酸钠的质量分数为_________.(已知: 5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O) 【答案】+34NaNO2 2Na2O+4NO↑+O2↑200NONaNO2+2Al+NaOH+H2O=2NaAlO2+NH3↑69% 【解析】 (1)根据在化合物中正负化合价代数和为零,可设亚硝酸钠中氮元素的化合价为x,则: (+1)+x+(-2)×2=0,解得x=+3,故答案为: +3; (2)因为亚硝酸钠在320℃时能分解产生氧化钠固体、一氧化氮气体和一种常见的助燃性气体,故反应的化学方程式为4NaNO2 2Na2O+4NO↑+O2↑; (3)因为我国规定肉灌肠中亚硝酸钠添加标准为每千克食品含量不超过150毫克,所以200g、15%的亚硝酸钠溶液至少可用于生产肉灌肠的质量为200g×15%÷ ═200kg,故答案为: 200kg; (6)消耗高锰酸钾的物质的量是0.1mol/L×0.02L=0.002mol,则根据方程式5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O可知,亚硝酸钠的物质的量是0.002mol× =0.005mol,则原样品中亚硝酸钠的物质的量是0.005mol× =0.02mol,其质量为0.02mol×69g/mol=1.38g,所以样品中亚硝酸钠的质量分数 ×100%=69.0%,故答案为: 69.0%。 9.【2018届河北区第一
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高考 化学 模拟 专题 13 元素 化合物 知识 综合 应用
 冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《畜牧学概论》复习题.docx
《畜牧学概论》复习题.docx
