 气体的等温变化玻意耳定律典型例题.docx
气体的等温变化玻意耳定律典型例题.docx
- 文档编号:11792186
- 上传时间:2023-06-02
- 格式:DOCX
- 页数:18
- 大小:341.84KB
气体的等温变化玻意耳定律典型例题.docx
《气体的等温变化玻意耳定律典型例题.docx》由会员分享,可在线阅读,更多相关《气体的等温变化玻意耳定律典型例题.docx(18页珍藏版)》请在冰点文库上搜索。
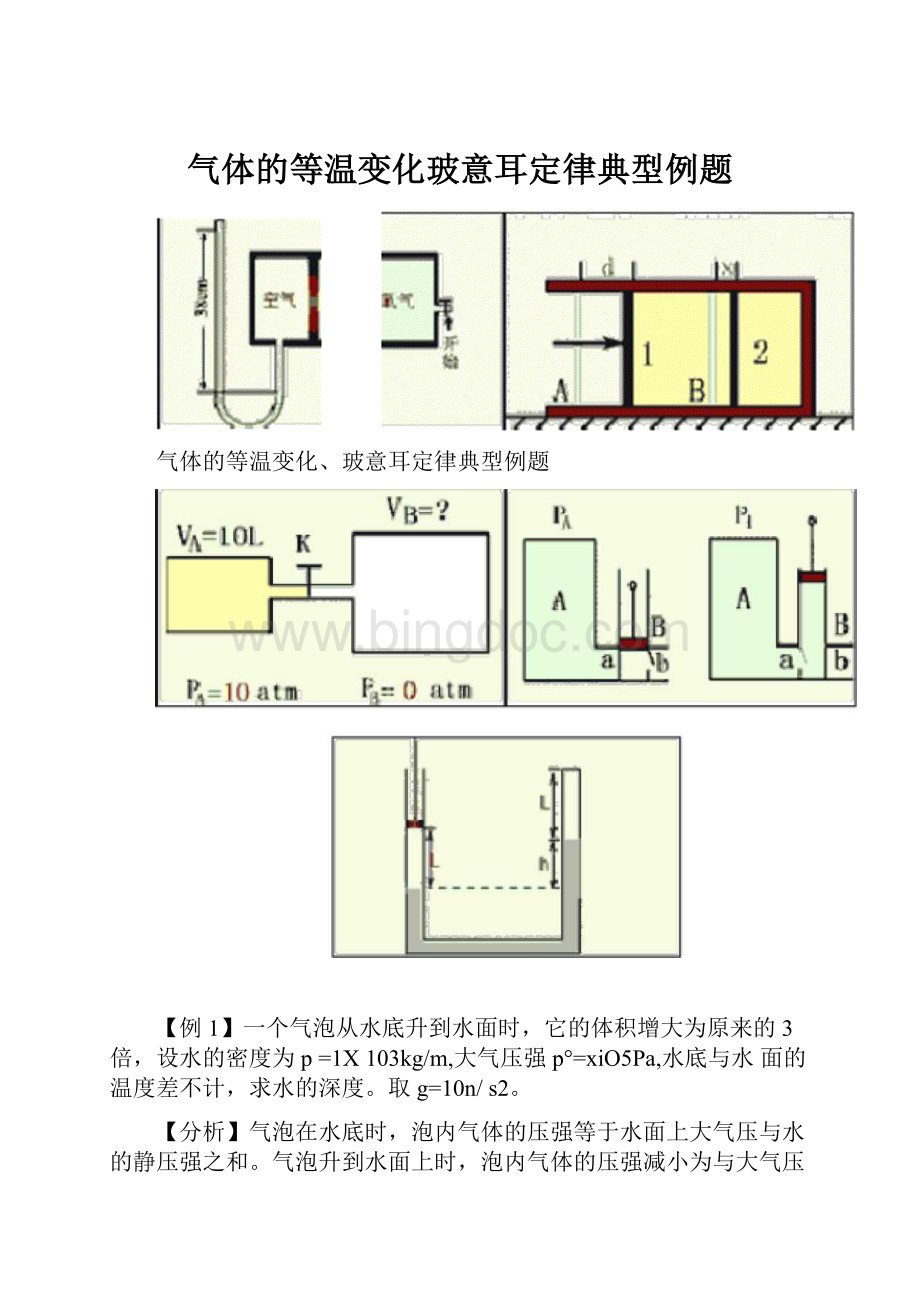
气体的等温变化玻意耳定律典型例题
气体的等温变化、玻意耳定律典型例题
【例1】一个气泡从水底升到水面时,它的体积增大为原来的3倍,设水的密度为p=1X103kg/m,大气压强p°=xiO5Pa,水底与水面的温度差不计,求水的深度。
取g=10n/s2。
【分析】气泡在水底时,泡内气体的压强等于水面上大气压与水的静压强之和。
气泡升到水面上时,泡内气体的压强减小为与大气压相等,因此其体积增大。
由于水底与水面温度相同,泡内气体经历的是一个等温变化过程,故可用玻意耳定律计算。
【解答】设气泡在水底时的体积为VI、压强为:
pi=p+pgh
气泡升到水面时的体积为V2,则V2=3V1压强为p2=pc
由玻意耳定律piV仁pV2,即
(po+pgh)V仁p•3V1
2X1.01X105
得水深
m-202m
【例2】如图1所示,圆柱形气缸活塞的横截面积为S,下表面与水平面的夹角为a,重量为G当大气压为po,为了使活塞下方密闭气体的体积减速为原来的1/2,必须在活塞上放置重量为多少的一个重物(气缸壁与活塞间的摩擦不计)
【误解】活塞下方气体原来的压强
设所加重物重为G,则活塞下方气体的压强变为
(G+Gf)cosCl
丹一內J心2
"S
气体体积减为原的1/2,则p=2p
cos0-
【正确解答】据图2,设活塞下方气体原来的压强为pi,由活塞
的平衡条件得
*cosa=p0S+GcosQ
国2
同理,加上重物G后,活塞下方的气体压强变为
G+&
叮=Po+—g—
气体作等温变化,根据玻意耳定律:
V
P1V=P2*V
得p2=2pi
G'=p)S+G
【错因分析与解题指导】【误解】从压强角度解题本来也是可以
的,但
將活塞产生的压强算成G发生了错误,这个压强值应该是G/S.为避
cosa
免发生以上关于压强计算的错误,相似类型的题目从力的平衡入手解题比较好。
在分析受力时必须注意由气体压强产生的气体压力应该垂直于接触面,气体压强乘上接触面积即为气体压力,情况就如【正确解答】所示。
【例3】一根两端开口、粗细均匀的细玻璃管,长L=30cm竖直
插入水银槽中深ho=1Ocm处,用手指按住上端,轻轻提出水银槽,并缓缓倒转,则此时管内封闭空气柱多长已知大气压R=75cmHg
【分析】插入水银槽中按住上端后,管内封闭了一定质量气体,
空气柱长L仁L-ho=2Ocm压强pi=po=75cmHg轻轻提出水银槽直立在
空气中时,有一部分水银会流出,被封闭的空气柱长度和压强都会发生变化。
设管中水银柱长h,被封闭气体柱长为L2=L-h。
倒转后,水银柱长度仍为h不变,被圭寸闭气体柱长度和压强又发生了变化。
设被封闭气体柱长L3
所以,管内封闭气体经历了三个状态。
由于“轻轻提出”、缓倒转”,意味着都可认为温度不变,因此可由玻意耳定律列式求解。
【解】根据上面的分析,画出示意图(图ab、c)。
气体所经
历的三个状态的状态参量如下表所示:
匡薩(ctiiHg)
体积(cm3J
(*)
PiG
耳广L臣
0
◎=95=(30-hJS
(c)
p^-75+h
由于整个过程中气体的温度不变,由玻意耳定律:
pVi=p2V2=pV>
75X20S=(75-h)(30-h)S=(75+h)L3S
由前两式得:
h2-105h+750=0
取合理解h=,代入得
75X201500
^=^TCfll=75777Cni=131ctU
【说明】必须注意题中隐含的状态(b),如果遗漏了这一点,将
无法正确求解。
【例4】容器A的容积是10L,用一根带阀门的细管,与容器B相连。
开始时阀门关闭,A内充有10atm的空气,B是真空。
后打开阀门把A中空气放一些到B中去,当A内压强降到4atm时,把阀门关闭,这时B内压强是3atm。
求容器B的容积。
假设整个过程中温度不变。
【分析】对流入容器B的这部分空气,它后来的状态为压强p'
B=3atm体积VB(容器B的容积)。
为了找出这部分空气的初态,可设想让容器A中的空气作等温膨胀,它的压强从10atm降为4atm时逸出容器A的空气便是进入B内的空气,于是即可确定初态。
【解答】先以容器A中空气为研究对象,它们等温膨胀前后的状态参量为:
V=10L,pA=10atm;
Va=,p'A=4atm。
由玻意耳定律paVA=P'aV'A,得
如图1所示
再以逸出容器A的这些空气为研究对象,它作等温变化前后的状
态为:
pi=p'A=4atm,V仁V'a-Va=15L
p'仁3atm,V'i=VB
同理由玻意耳定律piV仁p'iVB,得
Pl4=-15L=20L
BPt13
所以容器B的容积是20L。
【说明】本题中研究对象的选取至关重要,可以有多种设想。
例
如,可先以后来充满容器A的气体为研究对象(见图2)假设它原来
在容器A中占的体积为Vx,这部分气体等温变化前后的状态为:
團2
变化前:
压强pA=10atm、体积Vx,
变化后:
压强p'A=4atm体积Vx=V=10L。
由PaVx=p'aV'x
IJ
得兀-—X10L-4LPa1°
由此可见,进入B中的气体原来在A内占的体积为VA-Vx=(10-4)
L=6L。
再以这部分气体为研究对象,它在等温变化前后的状态为:
变化前:
压强pi=10atm,体积V1=6L,
变化后:
压强p2=3atm,体积V2=VB
由玻意耳定律得容器B的容积为:
V宜V!
-^X6L-20L
Pi
决定气体状态的参量有温度、体积、压强三个物理量,为了研究
这三者之间的联系,可以先保持其中一个量不变,研究另外两个量之间的关系,然后再综合起来。
这是一个重要的研究方法,关于气体性质的研究也正是按照这个思路进行的。
【例5】一容积为32L的氧气瓶充气后压强为13OON/cm2。
按规定当使用到压强降为100N/cm时,就要重新充气。
某厂每天要用400L氧气(在1atm下),一瓶氧气能用多少天(1atm=10N/crfi)设使用过程中温度不变。
【分析】这里的研究对象是瓶中的氧气。
由于它原有的压强
(1300N/cm),使用后的压强(100N/cm)、工厂应用时的压强(10N/cm)
都不同,为了确定使用的天数,可把瓶中原有氧气和后来的氧气都转
化为1atm,然后根据每天的耗氧量即可算出天数。
【解】作出示意图如图1所示。
根据玻意耳定律,由
piV仁p'1V1,pV2=p'2V'2
得
V;=竺叫=切出x32L=4160L
1Pi110
r(、
L300血■;/f气"Wcm3
Yi=3£L
\Jy7
\rl~-J
*_毎夭耗氧量
■vjPq—1OU/cm
-Vri=W0L
内=1OOIT/cm'
Va=—X32L=320L
32W
所以可用天数为:
4160-320
400
n■—=7--TT■96
【说明】根据上面的解题思路,也可以作其他设想。
如使后来留
在瓶中的氧气和工厂每天耗用的氧气都变成1300N/C祁的压强状态
下,或使原来瓶中的氧气和工厂每天耗用的氧气都变成100N/CR2的压
强状态下,统一了压强后,就可由使用前后的体积变化算出使用天数。
上面解出的结果,如果先用文字代入并注意到P'1=P'2=p。
,即
Pi“
“v?
~
pV仁pV2+npVO
这就是说,在等温变化过程中,当把一定质量的气体分成两部分
(或几部分),变化前后pV值之和保持不变(图2)。
这个结果,实
质上就是质量守恒在等温过程中的具体体现。
在气体的分装和混合等问题中很有用
【例6】如图所示,容器A的容积为VA=1OOL抽气机B的最大容积为VB=25L当活塞向上提时,阀门a打开,阀门b关闭;当活塞向下压时,阀门a关闭,阀门b打开。
若抽气机每分钟完成4次抽气动作,求抽气机工作多长时间,才能使容器A中气体的压强由70cmhg下降到(设抽气过程中容器内气体的温度不变)
【误解】设容器中气体等温膨胀至体积V2,压强由70cmHgF降
到,根据
pAVA=pV2
P2
vv
片畫怖wI--%_比_
70
(?
51)^100
八rn■—__"
VEVE
2^
9(决)
所需时间
34
t=—=85(nun)
【正确解答】设抽气1次后A中气体压强下降到p,根据
PaVA=p(VA+VB
得
第二次抽气后,压强为P2,则
XPa
同理,第三次抽气后,
抽气n次后,气体压强
代入数据得:
n=10(次)
所需时间=t=—=25(min)
4
【错因分析与解题指导】【误解】的原因是不了解抽气机的工作过程,认为每次抽入抽气机的气体压强均为。
事实上,每次抽气过程中被抽气体体积都是VB,但压强是逐步减小的,只是最后一次抽气时,压强才降低至。
因此,必须逐次对抽气过程列出玻意耳定律公式,再利用数学归纳法进行求解。
【例7】有开口向上竖直安放的玻璃管,管中在长h的水银柱下
方封闭着一段长L的空气柱。
当玻璃管以加速度a向上作匀加速运动
时,空气柱的长度将变为多少已知当天大气压为P。
,水银密度为P,
重力加速度为go
【误解】空气柱原来的压强为
pi=po+h
当玻璃管向上作匀加速动时,空气柱的压强为
速运动有
p2S-p°S-mg=ma
即p2=po+p(g+a)h
考虑空气的状态变化有
pLS=pL'S
p0
1/三*T
【正确解答】空气柱原来的压强为
pi=p)+pgh
P2,对水银柱的加
p2,由水银柱加
当玻璃管向上作匀加速运动时,空气柱的压强为速度运动得
p2S-p°S-mg=ma
p2=po+p(g+a)h
气体作等温变化
pLS=pL'S
解得V-
【错因分析与解题指导】本题是动力学和气体状态变化结合的综合题。
由于牛顿第二定律公式要求使用国际单位,所以压强的单位是“Pa”。
【误解】中pi=po+h,由动力学方程解得p2=p+p・(g+a)h,在压强的表示上,h和p(g+a)h显然不一致,前者以cmHg作单位是错误的。
所以在解答此类习题时,要特别注意统一单位,高为h的水
银柱的压强表达为p=pgh是解题中一个要点。
[例8]如图所示,内径均匀的U型玻璃管竖直放置,截面积为5cm,管右侧上端封闭,左侧上端开口,内有用细线栓住的活塞。
两管中分别封入L=11cm的空气柱A和B,活塞上、下气体压强相等为76cm水银柱产生的压强,这时两管内的水银面的高度差h=6cm现将活塞用
细线缓慢地向上拉,使两管内水银面相平。
求
(1)活塞向上移动的距离是多少
(2)需用多大拉力才能使活塞静止在这个位置上
[分析]两部分气体是靠压强来联系
U型玻璃管要注意水银面的变化,一端若下降xcm另一端必上升
xcm,两液面高度差为2xcm,由此可知,两液面相平,B液面下降h/2,
A管液面上升h/2在此基础上考虑活塞移动的距离
[解答]
(1)对于B段气体
8=76-6=70(cmHgpB2=p
y=11S(cm)VB2=(11+3)S(cmh)
根据玻意耳定律PBM=PB2VB2
7DX11S
-14S■芳伽晦
对于A段气体
pAi=76(cmHg)pA2=8=55(cmHg)
VAi=11s(cmb)VA2=L's(cm3)
根据玻意耳定律pAiV^i=pA2V^2
vPmVaiXH5
□p55
L'=152(cm)
对于活塞的移动距离:
h'=L'+3-L
=+3-11
=(cm)
(2)对于活塞平衡,可知
f+»2s=rs
F=RS-PS
[说明]U型管粗细相同时,一侧水银面下降hem另一侧水银面就
要上升hem,两部分液面高度差变化于2hem,若管子粗细不同,应该
从体积的变化来考虑,就用几何关系解决物理问题是常用的方法。
[例9]如图所示,在水平放置的容器中,有一静止的活塞把容器分隔成左、右两部分,左侧的容积是,存有空气;右侧的容积是3L,
存有氧气,大气压强是76cmHg先打开阀门K,当与容器中空气相连的U形压强计中左、右水银面的高度差减为19cm时,关闭阀K求后来氧气的质量与原来氧气的质量之比(系统的温度不变,压强计的容积以及摩擦不计)。
[分析]对于密圭寸的一定质量空气
初态
末态
p1=76+38(cmH^)
p/=76+19(cmH£)
V;=7
把原来容器中的氧气做为研究对象
初态
末态
p2=76+38(c
p严6+19[沁也)
Va=3L
V;=7
容器外(放走的)氧气体积厶V
△V=(Vi'+V2')-(V1+V)
在后来状态下,氧气密度相同
[解答]对于空气(温度不变)
对于氧气(温度不变)做为研究对象
容器外的氧气(假设仍处于末态)的体积
△v=(%小;)-GV也)
-(18+3.6)+
=0.9(L)
后来容器申氧气与原来氧气质量之出
可;■△V3.6-0.93
石=V;=35=4
[说明]:
理想气体的状态方程,是对一定量的气体而言,当它的状态发生变化时,状态参量之间的变化规律。
遵守气态方程。
而两部分气体时,要各自分别应用状态方程。
再通过力学条件,找到这两部分气之间压强或体积的关系。
本题容器内的氧气是属于变质量问题,也可以把它假想成质量不变来处理。
狀态1
状态2
气体单位体积的分子数相等,质量和体积成正比,可求得剩余质量(或放出的质量)与原质量之间的比例关系
求物体的质量可以用m=pV某个状态时的密度和该状态时体积的
乘积,而气态方程也可以写做密度形式
常用此式求某一状态时气体单位体积的分子数,然后再求气体的质量。
[例10]一横截面积为S的气缸水平放置,固定不动,气缸壁是导热的,两个活塞A和B将气缸分隔为1、2两气室,达到平衡时1、2两气室体积之比为3:
2,如图所示,在室温不变的条件下,缓慢推动活塞A,使之向右移动一段距离d,求活塞B向右移动的距离,不计活塞与气缸壁之间的摩擦。
[分析]气缸水平放置,不计活塞与气缸壁的摩擦,平衡时,两气室的压强必相等。
两气室各密封一定量的气体,缓慢推动活塞,故温度保持不变,分别运用玻意耳定律解题。
[解]因气缸水平放置,又不计活塞的摩擦,故平衡时两气室内的压强必相等,设初态时气室内压强为P0,气室1、2的体积分别为V
和V2;在活塞A向右移动d的过程中活塞B向右移动的距离为x;最后气缸内压强为p,因温度不变,分别对气室1和2的气体运用玻意耳定律,得
气室1poVi=p(Vi-Sd+Sx)①
气室2po"=p(V2-Sx)②
由①、②两式解得
[说明]气体实验定律,是研究某一定质量的气体,状态发生变化时,前、后状态参量变化的规律。
切不可理解为两部分气体状态参量的关系
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 气体 等温 变化 玻意耳 定律 典型 例题
 冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《初级会计实务》重点归纳.docx
《初级会计实务》重点归纳.docx
