 流程推断题.docx
流程推断题.docx
- 文档编号:10551630
- 上传时间:2023-05-26
- 格式:DOCX
- 页数:49
- 大小:1.24MB
流程推断题.docx
《流程推断题.docx》由会员分享,可在线阅读,更多相关《流程推断题.docx(49页珍藏版)》请在冰点文库上搜索。
流程推断题
评卷人
得分
二、填空题(题型注释)
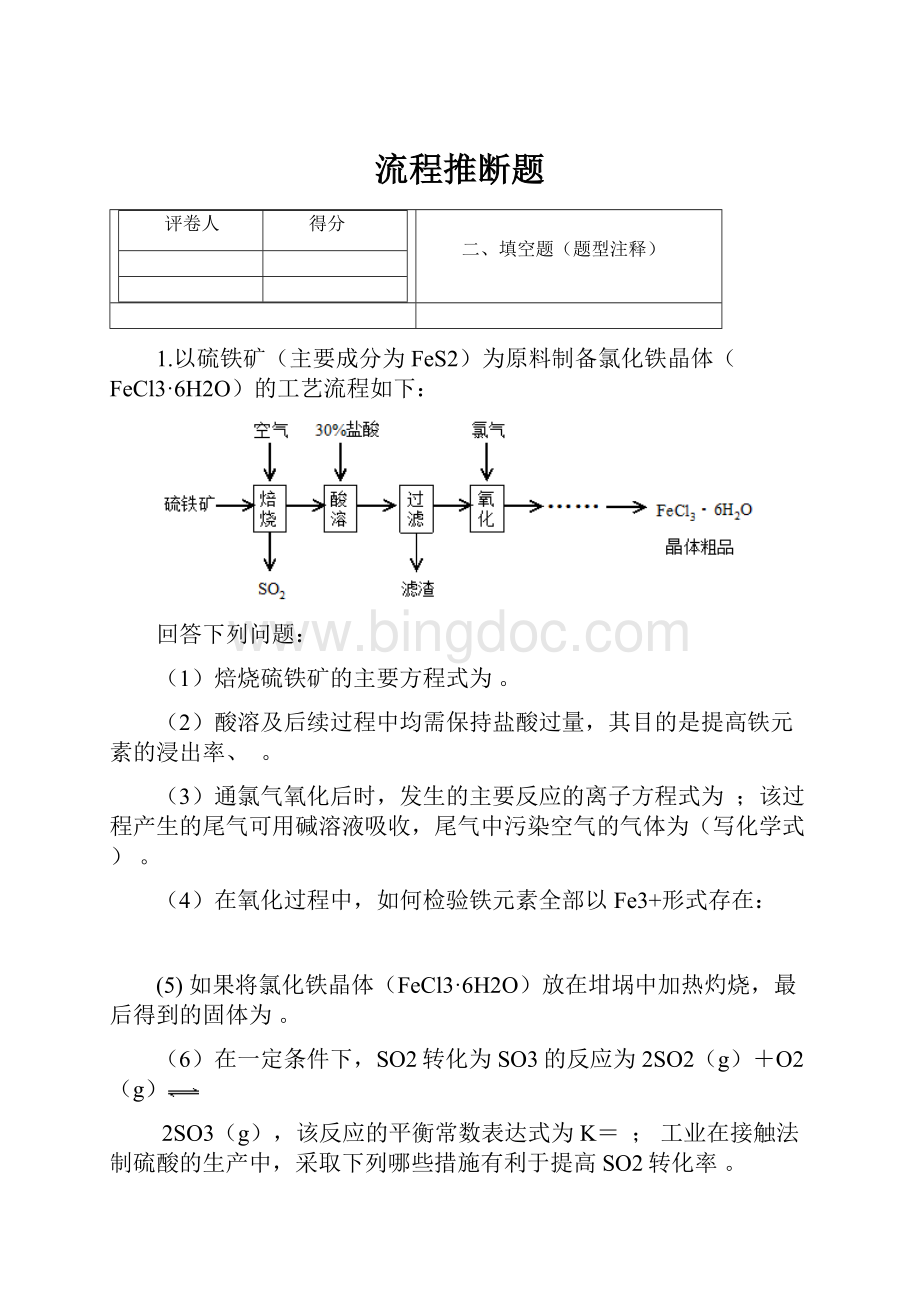
1.以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:
回答下列问题:
(1)焙烧硫铁矿的主要方程式为。
(2)酸溶及后续过程中均需保持盐酸过量,其目的是提高铁元素的浸出率、。
(3)通氯气氧化后时,发生的主要反应的离子方程式为;该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为(写化学式)。
(4)在氧化过程中,如何检验铁元素全部以Fe3+形式存在:
(5)如果将氯化铁晶体(FeCl3·6H2O)放在坩埚中加热灼烧,最后得到的固体为。
(6)在一定条件下,SO2转化为SO3的反应为2SO2(g)+O2(g)
2SO3(g),该反应的平衡常数表达式为K=;工业在接触法制硫酸的生产中,采取下列哪些措施有利于提高SO2转化率。
①V2O5作崔化剂②通入过量O2③SO2、O2进行二次氧化④通入过量SO2
答案:
1.
(1)4FeS2+11O2=2Fe2O3+8SO2(2分)
(2)抑制Fe3+水解(2分)(3)Cl2+Fe2+=2Cl-+Fe3+(2分)Cl2HCl(2分)
(4)取氧化后的溶液少许于试管中,往试管中滴加1~2滴酸性KMnO4溶液,KMnO4的紫红色不褪去,说明铁元素全部以Fe3+形式存在。
(2分)
(5)Fe2O3(2分)
(6)k=c2(SO3)/c(O2)·c2(SO2)(2分)②③(2分)
略
2.(16分)(
)下图是工业生产硝酸铵的流程。
(1)吸收塔C中通入空气的目的是。
A、B、C、D四个容器中的反应,属于氧化还原反应的是(填字母)。
(2)已知:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g)△H=-1266.8kJ/mol
N2(g)+O2(g)=2NO(g)△H=+180.5kJ/mol
写出氨高温催化氧化的热化学方程式:
(
)某合作小组同学将铜片加入稀硝酸,发现开始时反应非常慢,一段时间后反应速率明显加快。
该小组通过实验探究其原因。
(3)该反应的离子方程式为___________________________________________________。
(4)提出合理假设。
该实验中反应速率明显加快的原因可能是_____________________。
A.反应放热导致温度升高B.压强增大
C.生成物有催化作用D.反应物接触面积增大
(5)初步探究。
测定反应过程中溶液不同时间的温度,结果如下表:
时间/min
0
5
10
15
20
25
35
50
60
70
80
温度/℃
25
26
26
26
26
26
26.5
27
27
27
27
结合实验目的和表中数据,你得出的结论是__________________________________。
(6)进一步探究。
查阅文献了解到化学反应的产物(含中间产物)可能对反应有催化作用,请完成以下实验设计表并将实验目的补充完整:
实验
编号
铜片
质量/g
0.1mol·L-1的
硝酸体积/mL
硝酸铜
晶体/g
亚硝酸钠
晶体/g
实验目的
①
5
20
_______
_______
实验①和②探究_________的影响;实验①和③探究亚硝酸根的影响。
②
5
20
0.5
0
③
5
20
0
0.5
答案:
2.(
)
(1)使NO全部转化成HNO3(或提供O2氧化NO)(2分);ABC(2分)(少1个扣1分,多1个没有分)
(2)4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H=-905.8kJ/mol(3分)
(
)(3)3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O(3分)
(4)AC(2分)
(5)温度不是反应速率明显加快的主要原因。
(2分)
(6)(2分)
实验编号
铜片
质量/g
0.1mol·L-1的
硝酸体积/mL
硝酸铜
晶体/g
亚硝酸钠
晶体/g
实验目的
①
5
20
0
0
实验①和②探究
Cu2+的影响;实验①和③探究亚硝酸根的影响。
②
5
20
0.5
0
③
5
20
0
0.5
略
3.
答案:
3.
4.(13分)
二氧化铈
是一种重要的稀土氧化物。
平板电视显示屏生产过程中产生大量的废玻璃粉末(含
以及其他少量可溶于稀酸的物质)。
某课题组以此粉末为原料回收铈,设计实验流程如下:
(1)洗涤滤渣A的目的是为了去除(填离子符号),检验该离子是否洗涤的方法是。
(2)第②步反应的离子方程式是,滤渣B的主要成分是。
(3)萃取是分离稀土元素的常用方法,已知化合物TBP作为萃取剂能将铈离子从水溶液中萃取出来,TBP(填“能”或“不能”)与水互溶。
实验室进行萃取操作是用到的主要玻璃仪器有、烧杯、玻璃棒、量筒等。
(4)取上述流程中得到的
产品0.536g,加硫酸溶解后,用0.1000mol•
标准溶液滴定终点是(铈被还原为
),消耗25.00mL标准溶液,该产品中
的质量分数为。
答案:
4.
5.某盐卤矿抽出的废液中含有大量的K+、Cl—、Br—,及少量的Ca2+、Mg2+、SO42—。
某研究性学习小组拟取该废液来制取较纯净的氯化钾晶体及液溴(Br2),他们设计了如下流程:
现有可供选择的a、b试剂:
饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、H2O2、KMnO4(H+)溶液、稀HNO3。
请根据以上流程,回答相关问题:
(1)试剂a应选_____,该反应在酸性环境中完成,其离子方程式为。
(2)操作①、②、③、④、⑤的名称依次为_________(选填字母)。
A.萃取、过滤、分液、过滤、蒸发结晶B.萃取、分液、分液、过滤、蒸发结晶
C.分液、萃取、过滤、过滤、蒸发结晶D.萃取、分液、蒸馏、过滤、蒸发结晶
(3)操作⑤中用到的瓷质仪器名称是。
(4)选出除去无色液体I中Ca2+、Mg2+、SO42-离子所需的试剂,按滴加顺序依次为(填化学式)。
(5)调节pH的作用是。
答案:
5.
6.以食盐为原料进行生产并综合利用的某些过程如下图所示。
(1)除去粗盐中的Ca2+、Mg2+和SO
离子,加入下列沉淀剂的顺序是(填序号)。
a.Na2CO3b.NaOHc.BaCl2
(2)将滤液的pH调至酸性除去的离子是。
(3)电解饱和食盐水反应的离子方程式是。
(4)若向分离出NaHCO3晶体后的母液中加入过量生石灰,则可获得一种可以循环使用的物质,其化学式是。
(5)纯碱在生产生活中有广泛的应用。
①纯碱可用于除灶台油污。
其原因是(结合离子方程式表述)。
②常温下,向某pH=11的Na2CO3溶液中加入过量石灰乳,过滤后所得溶液pH=13。
则反应前的溶液中与反应后的滤液中水电离出的c(OH—)的比值是。
③工业上,可以用纯碱代替烧碱生产某些化工产品。
如用饱和纯碱溶液与Cl2反应制取有效成分为NaClO的消毒液,其反应的离子方程式是。
(已知碳酸的酸性强于次氯酸)。
答案:
6.
(1)cab或者cba或者bca
(2)CO
和OH—
(3)2Cl-+2H2O
2OH-+H2↑+Cl2↑(4)NH3
(5)①CO
水解显碱性CO
+H2O
HCO
+OH—,油污在碱性条件下水解,达到去污目的。
②1×1010③2CO
+Cl2+H2O=Cl—+ClO—+2HCO
略
7.某厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子。
有人设计了图中的工艺流程,利用常用的酸、碱和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。
填写下面空白。
(1)图中标号处需加入的相应物质分别是① 、② 、③ 、④ 、⑤ ;
(2)写出①处发生反应的离子方程式 ;写出③处发生反应的化学方程式 ;
(3)铁红的化学式为 ;分别写出铁红和氧化铜在工业上的一种主要用途:
铁红 。
答案:
7.
(1)①铁屑②稀硫酸③稀硝酸④氢氧化钠⑤氨水(其他合理答案均可)
(2)①处Fe+2H+=Fe2++H2↑2Fe3++Fe=3Fe2+
Cu2++Fe=Cu+Fe2+2Au3++3Fe=2Au+3Fe2+
③处3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
(3)氧化铁(Fe2O3),做红色涂料(其他合理答案均可)。
略
8.回收再利用锗产品加工废料,是生产GeO2的重要途径,其流程如下图。
(1)Ge2+与氧化剂H2O2反应生成Ge4+,写出该反应的离子方程式:
。
(2)蒸馏可获得沸点较低的GeCl4,在此过程中加入浓盐酸的原因是:
。
(3)GeCl4水解生成GeO2·nH2O,此过程用化学方程式可表示为:
。
温度对GeCl4的水解率产生的影响如图所示。
为控制最佳的反应温度,实验时可采取的措施为。
(填序号)
A.用冰水混合物
B.49℃水浴
C.用冰盐水
(4)Ge位于元素周期表第四周期第IVA族,根据下表中不同pH下二氧化锗的溶解率,结合“对角线”法则,分析GeO2溶解率随pH变化的原因 ,用离子方程式表示pH>8时GeO2溶解率增大可能发生的反应。
不同pH下二氧化锗的溶解率
pH
4
5
6
7
8
9
10
溶解率/%
47.60
32.53
11.19
5.27
1.96
8.85
19.23
答案:
8.
(1)Ge2++H2O2+2H+=Ge4++2H2O
(2)抑制GeCl4水解
(3)GeCl4+(2+n)H2O=GeO2·nH2O+4HC1C
(4)二氧化锗具有两性(或属于两性氧化物);GeO2+2OH-=GeO
+H2O
略
9.10分)过氧化钙可以用于改善地表水质、处理含重金属粒子废水和治理赤潮,也可用于应急供氧等。
工业上生产过氧化钙的主要流程如下:
已知CaO2·8H2O呈白色,微溶于水,加热至350℃左右开始分解放出氧气。
(1)用上述方法制取CaO2·8H2O的化学方程式是;
(2)沉淀时常用冰水控制温度在0℃左右,其可能原因是(写出两种):
①;
②。
(3)测定产品中CaO2的含量的实验步骤是:
第一步:
准确称取ag产品于有塞锥形瓶中,加入适量蒸馏水和过量的bgKI晶体,再滴入少量2mol/L的H2SO4溶液,充分反应。
第二步:
向上述锥形瓶中加入几滴淀粉溶液。
第三步:
逐滴加入浓度为cmol·L—1的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液VmL。
【已知:
I2+2S2O32-=2I-+S4O62-】
①CaO2的质量分数为(用字母表示);
②某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的CaO2的质量分数可能(填“不受影响”、“偏低”或“偏高”),原因是_______________。
答案:
9.(10分)
(1)CaCl2+H2O2+2NH3+8H2O=CaO2·8H2O↓+2NH4Cl(2分)
(2)①温度低可减少过氧化氢的分解,提高过氧化氢的利用率(1分);
②该反应是放热反应,温度低有利于提高CaO2·8H2O产率(1分)。
(3)①
,(2分)
②偏高(2分),在酸性条件下空气中的O2也可以把KI氧化为I2,使消耗的Na2S2O3
增多,从而使测得的CaO2的质量分数偏高。
(2分)
略
10.工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下:
(1)气体A中的大气污染物可选用下列试剂中的________吸收。
a.浓H2SO4 b.稀HNO3c.NaOH溶液d.氨水
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在________(填离子符号),检验溶液中还存在Fe2+的方法是
(注明试剂、现象)。
(3)由泡铜(主要成分为Cu2O、Cu)冶炼粗铜的化学反应方程式
为_________________。
答案:
10.
(1)c、d
(2)Fe3+ 取少量溶液,滴加KMnO4溶液,KMnO4褪色,则溶液
中存在Fe2+(3)3Cu2O+2AlAl2O3+6Cu
略
11.工业废水中常含有一定量的
和
,它们会对人类及生态系统产生很大的伤害,必须进行处理。
常用的处理方法有两种。
方法1:
还原沉淀法:
该法的工艺流程为
其中第①步存在平衡:
CrO
(黄色)+2H+=Cr
O
(橙色)+2H2O
(1)若平衡体系的pH=2,则溶液显色.
(2)能说明第①步反应达平衡状态的是。
a.Cr
O
和CrO
的浓度相同
b.2v(Cr
O
)=v(CrO
)
c.溶液的颜色不变
(3)第②步中,还原1molCr
O
离子,需要mol的FeSO
·7H
O。
(4)第③步生成的Cr(OH)
在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(aq)
Cr3+(aq)+3OH-(aq)
常温下,Cr(OH)
的溶度积
,要使
降至10
mol/L,溶液的pH应调至。
方法2:
电解法:
该法用Fe做电极电解含
的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)
沉淀。
(5)用Fe做电极的原因为发生(用电极反应解释)而提供。
(6)在阴极附近溶液pH升高的原因是(用电极反应解释)。
溶液中同时生成的沉淀还有。
答案:
11.
(1)橙
(2)C(3)6(4)5
(5)Fe-2e-=Fe2+Fe2+
(6)2H++2e-==H2↑Fe(OH)3
略
12.二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的消毒剂,是一种黄绿色的气体,易溶于水。
Ⅰ.ClO2可由KClO3在H2SO4存在的条件下与Na2SO3反应制得。
则该反应的氧化产物与还原产物的物质的量之比是 。
Ⅱ.实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程如下:
(1)写出电解时发生反应的化学方程式:
;
(2)除去ClO2中的NH3可选用的试剂是;(填序号)
A.饱和食盐水B.碱石灰C.浓硫酸D.水
(3)测定ClO2的过程如下:
在锥形瓶中加入足量的碘化钾,用100mL水溶解后,再加3mL硫酸溶液,将生成的ClO2气体通入锥形瓶中充分反应。
再加入几滴淀粉溶液,用cmol/L硫代硫酸钠标准溶液滴定(I2+2S2O32-=2I-+S4O62-),共用去VmL硫代硫酸钠溶液。
①请写出上述二氧化氯气体与碘化钾溶液反应的离子方程式 ;
②滴定终点的现象是:
。
③测得通入ClO2的质量m(ClO2)=。
(用含c、V的代数式表示)
答案:
12.
(1)1:
2
(2)NH4Cl+2HCl
3H2↑+NCl3
(2)C
(3)①2ClO2+10I-+8H+=4H2O+5I2+2Cl-
②最后一滴滴下时,溶液由蓝色变为无色,且半分钟内不复原
③1.35cv×10-2g
略
13.以下是FeSO4•7H2O的实验室制备流程图。
根据题意完成下列填空:
(1).碳酸钠溶液能除去酯类油污,是因为(用离子方程式表示),反应Ⅰ需要加热数分钟,其原因是。
(2).废铁屑中含氧化铁,无需在制备前除去,理由是(用离子方程式回答)
,。
(3).判断反应Ⅱ完成的现象是:
。
以下是测定某补血剂(FeSO4•7H2O)中铁元素含量的流程图。
根据题意完成下列填空:
Ⅲ
(4).步骤Ⅲ需要100mL1mol/L的稀硫酸,用98.3%,ρ=1.84g/cm3的浓硫酸配制,所用的仪器有量筒、烧杯、玻璃棒、胶头滴管及。
(5).步骤Ⅴ一系列操作依次是:
①过滤②洗涤③④冷却⑤称量⑥恒重操作。
(6).假设实验无损耗,则每片补血剂含铁元素的质量g(用含a的代数式表示)。
答案:
13.
(1).CO32—+H2O
HCO3—+2OH—;升温,促进水解,溶液碱性增强,使反应充分进行。
(合理即可)
(2).Fe2O3+6H+→2Fe3++3H2O,2Fe3++Fe→3Fe2+2、
(3).铁粉不再溶解,铁粉表面不再有气泡产生
(4).100mL容量瓶(5).③灼烧(加热)(6).0.07a
略
14.信息时代产生的大量电子垃圾对环境构成了极大的威胁。
某探究小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
请回答下列问题:
(1)得到滤渣1的主要成分为。
(2)第②步加H2O2的作用是,使用H2O2的优点是,调溶液pH的目的是使
生成沉淀。
(3)操作3的名称是、、。
(4)由滤渣2制取Al2(S04)3·18H2O,探究小组设计了三种方案:
上述三种方案中,方案不可行,原因是
。
从原子利用率角度考虑,方案更合理。
答案:
14.
(l)Au、Pt
(2)将Fe2+氧化为Fe3+不引入杂质,对环境无污染Fe3+、Al3+
(3)蒸发浓缩、冷却结晶、过滤
(4)甲所得产品中含有较多Fe2(SO4)3杂质乙
略
15.铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题:
(1)生铁中含有一种铁碳化合物X(Fe3C)。
X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸的溶液中含有的大量阳离子是________________________。
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等四种离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入到过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是________;
A.Mg2+ B.Fe2+
C.Al3+D.Cu2+
(3)氧化铁是重要工业颜料,用废铁屑制备它的流程如下:
回答下列问题:
①操作Ⅰ、Ⅱ的名称分别是____、____。
②写出在空气中煅烧FeCO3的化学方程式;
(4)有些同学认为KMnO4溶液滴定也能进行铁元素含量的测定(5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O)。
a.称取2.850g绿矾(FeSO4·7H2O)产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需_______________。
②计算上述样品中FeSO4·7H2O的质量分数为。
答案:
15.
(1)Fe2+、Fe3+、H+
(2)B、C
(3)①过滤、洗涤(2分) ②4FeCO3+O2
2Fe2O3+4CO2
(4)①250mL容量瓶 ②0.9754
略
16.难溶性杂卤石(K2SO4·MgSO4·2CaSO4·2H2O)属于“呆矿”,在水中存在如下平衡
为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,工艺流程如下:
(1)滤渣主要成分有和以及未溶杂卤石。
(2)用化学平衡移动原理解释Ca(OH)2溶液能溶解杂卤石浸出K+的原因:
。
(3)“除杂”环节中,先加入溶液,经搅拌等操作后,过滤,再加入溶液调滤液PH至中性。
(4)不同温度下,K+的浸出浓度与溶浸时间的关系是图14,由图可得,随着温度升高,
①在相同时间K+的浸出浓度大。
②在相同时间K+的浸出浓度减小
③反应的速率加快,平衡时溶浸时间短。
④反应速率减慢,平衡时溶浸时间增长。
(5)有人以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:
已知298K时,Ksp(CaCO3)=2.80×10—9,Ksp(CaSO4)=4.90×10—5,求此温度下该反应的平衡常数K。
答案:
16.
(1)CaSO4Mg(OH)2
(2)氢氧根与镁离子结合,使平衡向右移动,K+变多。
(3)K2CO3H2SO4
(4)①③
(5)K=1.75×104
略
17.聚合氯化铝晶体的化学式为[Al2(OH)nCl6-n·XH2O]m,它是一种高效无机水处理剂,它的制备原理是调节增大AlCl3溶液的pH,通过促进其水解而结晶析出。
其制备原料主要是铝加工行业的废渣——铝灰,它主要含Al2O3、Al,还有SiO2等杂质。
聚合氯化铝生产的工艺流程如下:
(1)反应中副产品a是。
(2)生产过程中操作A和操作B(填“是”或“否”)相同,有人建议在用清水清洗后也应该进行操作A,你认为他的建议(填“是”或“否”)合理,理由是,操作A过程中使用到的主要玻璃仪器有。
(3)调节pH至4.0~4.5的目的是。
(4)实验室要测定水处理剂产品中n和x的值。
为使测定结果更准确,需得到纯净的晶体。
生产过程C中可选用的物质为(填字母代号)。
A.NaOHB.AlC.氨水D.Al2O3
答案:
17.
(1)H2;
(2)是;否;不过滤也不会引入杂质,若清水清洗后过滤,同时会把单质铝过滤出来,使原料损失,产率降低;漏斗、烧杯和玻璃棒;
(3)促进AlCl3水解,使晶体析出。
(4)BD
略
18.镁砂(MgO)是一种高温耐火材料。
下图是氨法制取高纯镁砂的部分工艺流程:
请回答:
(1)MgCl2•6H2O溶于水,溶液呈(填“酸性”.“中性”.或“碱性”)。
(2)写出氨分子的电子式。
(3)蒸氨是将石灰乳加入氯化铵溶液中,并加热,写出该反应的化学方程式:
。
(4)轻烧后的产物为。
(5)工业获取的MgCl2•6H2O常混有FeCl3,除去MgCl2溶液中的Fe3+,可选用下列试剂
A.MgO B.NaOH C.Mg(OH)2D.KSCN
(6)氨化反应过程中反应的离子方程式。
(7)过滤洗涤主要是除去附着在固体表面的氯离子,检验沉淀已洗涤干净的方法是。
答案:
18.
(1)酸性
(2)
(3)Ca(OH)2+2NH4Cl
2NH3↑+CaCl2+2H2O
(4)MgO(或氧化镁)
(5)AC
(6)Mg2++2NH3+2H2O=Mg(OH)
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 流程 推断
 冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰点文库所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《大侦探小卡莱》读后感.docx
《大侦探小卡莱》读后感.docx
